
Structura, proprietățile, nomenclatura și utilizările alcoolilor
alcooli sunt compuși organici care se caracterizează prin faptul că au o grupare hidroxil (-OH) legată de un carbon saturat; adică un carbon care este legat de patru atomi prin legături simple (fără legături duble sau triple).
Formula generică pentru această vastă și versatilă familie de compuși este ROH. Pentru a fi considerat alcool în sens strict chimic, grupul OH trebuie să fie cel mai reactiv din structura moleculară. Acest lucru este important pentru a putea afirma, printre mai multe molecule cu grupări OH, care dintre ele este un alcool..

Unul dintre alcoolii prin excelență și cel mai cunoscut în cultura populară este alcoolul etilic sau etanolul, CH3CHDouăOH. În funcție de originea lor naturală și, prin urmare, de mediul lor chimic, amestecurile lor pot provoca un spectru nelimitat de arome; unele, care arată chiar schimbări pozitive la nivelul palatului odată cu zborul anilor.
Sunt amestecuri de compuși organici și anorganici cu alcool etilic, ceea ce dă naștere consumului său în evenimente sociale și religioase din timpuri înainte de Hristos; cum ar fi cu vin de struguri sau cu pahare servite pentru o sărbătoare, pe lângă pumni, bomboane, panettone etc..
Plăcerea acestor băuturi, cu măsură, este rezultatul sinergiei dintre alcoolul etilic și matricea sa chimică învelitoare; fără ea, ca substanță pură, devine extrem de periculoasă și declanșează o serie de consecințe negative asupra sănătății.
Din acest motiv, consumul de amestecuri apoase de CH3CHDouăOH, ca și cele cumpărate în farmacii în scopuri antiseptice, reprezintă un mare risc pentru organism.
Alți alcooli care sunt, de asemenea, foarte populari sunt mentolul și glicerolul. Acesta din urmă, precum și eritrolul, se găsește ca aditiv în multe alimente pentru îndulcirea și conservarea lor în timpul depozitării. Există entități guvernamentale care dictează ce alcooli pot fi folosiți sau consumați fără efecte colaterale..
Lăsând în urmă utilizarea zilnică a alcoolilor, chimic sunt substanțe foarte versatile, deoarece începând de la aceștia, pot fi sintetizați și alți compuși organici; până la punctul în care unii autori cred că cu o duzină dintre aceștia pot fi creați toți compușii necesari pentru a trăi pe o insulă pustie.
Indice articol
- 1 Structura alcoolilor
- 1.1 Caracter amfifilic
- 1.2 Structura lui R
- 2 Proprietăți fizice și chimice
- 2.1 Punctul de fierbere
- 2.2 Capacitatea solventului
- 2.3 Amfotericism
- 3 Nomenclatură
- 3.1 Denumire comună
- 3.2 Sistemul IUPAC
- 4 Sinteza
- 4.1 Hidratarea alchenelor
- 4.2 Procesul Oxo
- 4.3 Fermentarea glucidelor
- 5 utilizări
- 5.1 Băuturi
- 5.2 Materie primă chimică
- 5.3 Solvenți
- 5.4 Combustibili
- 5.5 Antiseptice
- 5.6 Alte utilizări
- 6 Referințe
Structura alcoolilor
Alcoolii au o formulă generală de ROH. Gruparea OH este legată de gruparea alchil R, a cărei structură variază de la un alcool la altul. Uniunea dintre R și OH se face printr-o legătură covalentă simplă, R-OH.
Imaginea următoare prezintă trei structuri generice pentru alcooli, ținând cont de faptul că atomul de carbon este saturat; adică formează patru legături simple.
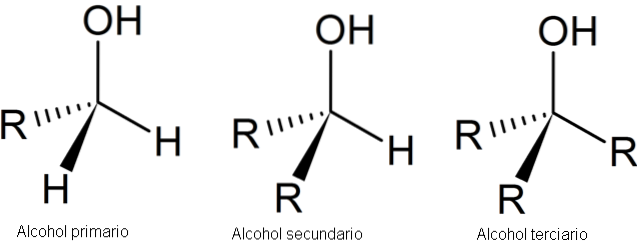
După cum se poate vedea, R poate fi orice schelet de carbon atâta timp cât nu are substituenți mai reactivi decât gruparea OH..
În cazul alcoolului primar, în primul rând, grupul OH este legat de un carbon primar. Acest lucru se verifică ușor observând că atomul din centrul tetraedrului stâng este legat de un R și doi H.
Alcoolul secundar, 2º, este verificat cu carbonul tetraedrului din centru legat acum de două grupe R și unul H.
Și, în cele din urmă, există alcoolul terțiar, 3º, cu carbonul legat de trei grupe R.
Personaj amfifilic
În funcție de tipul de carbon legat de OH, există clasificarea alcoolilor primari, secundari și terțiari. În tetraedre, diferențele structurale dintre ele au fost deja detaliate. Dar, toți alcoolii, indiferent de structura lor, împărtășesc ceva în comun: caracterul amfiphilic..
Nu trebuie să abordați o structură pentru a o observa, ci doar formula sa ROH. Gruparea alchil este alcătuită aproape în întregime din atomi de carbon, „asamblând” o coloană vertebrală hidrofobă; adică interacționează foarte slab cu apa.
Pe de altă parte, grupul OH poate forma legături de hidrogen cu moleculele de apă, fiind astfel hidrofil; adică iubește sau are o afinitate pentru apă. Deci, alcoolii au o coloană vertebrală hidrofobă, atașată la un grup hidrofil. Ele sunt apolare și polare în același timp, ceea ce înseamnă că sunt substanțe amfifile.
R-OH
(Hidrofob) - (Hidrofil)
După cum se va explica în secțiunea următoare, caracterul amfifilic al alcoolilor definește unele dintre proprietățile lor chimice..
Structura lui R
Gruparea alchil R poate avea orice structură și totuși este importantă, deoarece permite catalogarea alcoolilor.
De exemplu, R poate fi un lanț deschis, cum este cazul etanolului sau propanolului; ramificat, cum ar fi alcoolul t-butilic, (CH3)DouăCHCHDouăOH; poate fi ciclic, ca în cazul ciclohexanolului; sau poate avea un inel aromatic, ca în alcoolul benzilic (C6H5) CHDouăOH, sau în 3-fenilpropanol, (C6H5) CHDouăCHDouăCHDouăOh.
Lanțul R poate avea chiar substituenți precum halogeni sau legături duble, cum ar fi pentru alcooli 2-cloroetanol și 2-buten-1-ol (CH3CHDouă= CHCHDouăOH).
Având în vedere structura lui R, clasificarea alcoolilor devine complexă. Din acest motiv, clasificarea pe baza structurii lor (1, 2 și 3 alcooli) este mai simplă, dar mai puțin specifică, deși este suficientă pentru a explica reactivitatea alcoolilor..
Proprietati fizice si chimice
Punct de fierbere
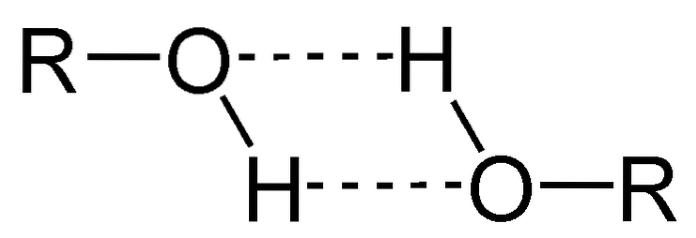
Una dintre principalele proprietăți ale alcoolilor este că se asociază prin legături de hidrogen.
În imaginea de mai sus, puteți vedea cum două molecule ROH formează legături de hidrogen între ele. Datorită acestui fapt, alcoolii sunt de obicei lichide cu puncte de fierbere ridicate..
De exemplu, alcoolul etilic are un punct de fierbere de 78,5 ° C. Această valoare crește pe măsură ce alcoolul devine mai greu; adică grupul R are o masă sau un număr mai mare de atomi. Astfel, alcoolul n-butilic, CH3CHDouăCHDouăCHDouăOH, are un punct de fierbere de 97 ° C, ușor mai mic decât cel al apei.
Glicerolul este unul dintre alcoolii cu cel mai înalt punct de fierbere: 290ºC.
De ce? Deoarece nu numai masa sau structura influențelor R, ci și numărul grupelor OH. Glicerolul are trei OH în structura sa: (HO) CHDouăCH (OH) CHDouă(OH). Acest lucru îl face capabil să formeze multe legături de hidrogen și să-și țină moleculele împreună mai strâns..
Pe de altă parte, unii alcooli sunt solizi la temperatura camerei; ca același glicerol la o temperatură sub 18 ° C. Prin urmare, afirmația că toți alcoolii sunt substanțe lichide este incorectă..
Capacitatea solventului
În case este foarte obișnuit să recurgi la utilizarea alcoolului izopropilic pentru a îndepărta o pată greu de îndepărtat pe o suprafață. Această capacitate de solvent, foarte utilă pentru sinteza chimică, se datorează caracterului său amfifilic, explicat anterior.
Grăsimile se caracterizează prin faptul că sunt hidrofobe: de aceea este dificil să le îndepărtați cu apă. Cu toate acestea, spre deosebire de apă, alcoolii au o parte hidrofobă în structura lor.
Astfel, gruparea sa alchil R interacționează cu grăsimile, în timp ce gruparea OH formează legături de hidrogen cu apa, ajutând la deplasarea lor..
Amfotericism
Alcoolii pot reacționa ca acizi și baze; adică sunt substanțe amfotere. Aceasta este reprezentată de următoarele două ecuații chimice:
ROH + H+ => ROHDouă+
ROH + OH- => RO-
RO- este formula generală a ceea ce este cunoscut sub numele de alcoxid.
Nomenclatură
Există două moduri de numire a alcoolilor, a căror complexitate va depinde de structura lor.
Denumirea comună
Alcoolii pot fi numiți după numele lor comune. Care sunt? Pentru aceasta, trebuie cunoscut numele grupului R, la care se adaugă terminația -ico și este precedat de cuvântul „alcool”. De exemplu, CH3CHDouăCHDouăOH este alcool propilic.
Alte exemple sunt:
-CH3OH: alcool metilic
-(CH3)DouăCHCHDouăOH: alcool izobutilic
-(CH3)3COH: alcool terț-butilic
Sistemul IUPAC
În ceea ce privește numele comune, trebuie să începeți prin identificarea R. Avantajul acestui sistem este că este mult mai precis decât celălalt..
R, fiind un schelet de carbon, poate avea ramuri sau mai multe lanțuri; cel mai lung lanț, adică cu mai mulți atomi de carbon, este cel care va primi numele de alcool.
La numele alcanului celui mai lung lanț se adaugă terminația „l”. De aceea la CH3CHDouăOH se numește etanol (CH3CHDouă- + OH).
În general, OH ar trebui să aibă cea mai mică enumerare posibilă. De exemplu, BrCHDouăCHDouăCHDouă(OH) CH3 se numește 4-bromo-2-butanol și nu 1-bromo-3-butanol.
Sinteză
Hidratarea alcenelor
Procesul de cracare a uleiului produce un amestec de alchene de patru sau cinci atomi de carbon, care pot fi ușor separate.
Aceste alchene pot fi transformate în alcooli prin adăugarea directă de apă sau prin reacția alchenei cu acidul sulfuric, urmată de adăugarea apei care scindează acidul, originând alcoolul..
Procesul Oxo
În prezența unui catalizator adecvat, alchenele reacționează cu monoxid de carbon și hidrogen pentru a genera aldehide. Aldehidele pot fi ușor reduse la alcooli printr-o reacție de hidrogenare catalitică.
Adesea există o astfel de sincronizare a procesului oxo încât reducerea aldehidelor este aproape simultană cu formarea lor..
Cel mai utilizat catalizator este dicobalt octocarbonil, obținut prin reacția dintre cobalt și monoxid de carbon.
Fermentarea carbohidraților
Fermentarea carbohidraților prin drojdie este încă de o mare importanță în producția de etanol și alți alcooli. Zaharurile provin din trestie de zahăr sau amidon obținute din diferite boabe. Din acest motiv, etanolul mai este numit „alcool din cereale”
Aplicații
Băuturi
Deși nu este funcția principală a alcoolilor, prezența etanolului în unele băuturi este una dintre cele mai populare cunoștințe. Astfel, etanolul, un produs al fermentării trestiei de zahăr, strugurilor, merelor etc., este prezent în numeroase băuturi destinate consumului social..
Materie primă chimică
-Metanolul este utilizat în producția de formaldehidă, prin oxidarea sa catalitică. Formaldehida este utilizată la fabricarea materialelor plastice, a vopselelor, a textilelor, a explozivilor etc..
-Butanolul este utilizat în producția de butan etanoat, un ester utilizat ca aromă în industria alimentară și de cofetărie..
-Alcoolul alilic este utilizat în producția de esteri, inclusiv ftalat de dialil și izoftalat de dialil, care servesc drept monomeri.
-Fenolul este utilizat în producția de rășini, fabricarea nailonului, deodorante, produse cosmetice etc..
-Alcoolii cu un lanț drept de 11-16 atomi de carbon sunt folosiți ca intermediari pentru a obține plastifianți; de exemplu, clorura de polivinil.
-Așa-numiții alcooli grași sunt folosiți ca intermediari în sinteza detergenților.
Solvenți
-Metanolul este utilizat ca diluant de vopsea, la fel ca 1-butanolul și alcoolul izobutilic.
-Alcoolul etilic este utilizat ca solvenți pentru mulți compuși insolubili în apă, fiind utilizat ca solvent în vopsele, produse cosmetice etc..
-Alcoolii grași sunt folosiți ca solvenți în industria textilă, în coloranți, în detergenți și în vopsele. Isobutanolul este utilizat ca solvent în materialele de acoperire, vopsele și adezivi.
Combustibili
-Metanolul este utilizat ca combustibil în motoarele cu ardere internă și ca aditiv pe benzină pentru a îmbunătăți arderea.
-Alcoolul etilic este utilizat în combinație cu combustibili fosili în autovehicule. În acest scop, regiuni extinse din Brazilia sunt destinate cultivării trestiei de zahăr pentru producția de alcool etilic. Acest alcool are avantajul de a produce numai dioxid de carbon în arderea sa..
Când alcoolul etilic este ars, acesta produce o flacără curată, fără fum, motiv pentru care este folosit ca combustibil în bucătăriile de câmp..
-Alcoolul gelificat este produs prin combinarea metanolului sau etanolului cu acetat de calciu. Acest alcool este utilizat ca sursă de căldură în sobele de câmp și, din moment ce se varsă, este mai sigur decât alcoolii lichizi.
-Așa-numitul biobutanol este utilizat ca combustibil în transport, precum și alcoolul izopropilic care poate fi folosit ca combustibil; deși nu se recomandă utilizarea acestuia.
Antiseptice
Alcoolul izopropilic la concentrație de 70% este utilizat ca antiseptic extern pentru a elimina germenii și a întârzia creșterea acestora. De asemenea, alcoolul etilic este utilizat în acest scop..
Alte utilizări
Ciclohexanolul și metilciclohexanolul sunt utilizate în finisarea textilelor, prelucrarea mobilierului și îndepărtarea petelor.
Referințe
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimie organica. Amine. (10a ediție.). Wiley plus.
- Carey F. (2008). Chimie organica. (Ediția a șasea). Mc Graw Hill.
- Morrison și Boyd. (1987). Chimie organica. (Ediția a cincea). Addison-Wesley Iberoamericana.
- Dr. JA Colapret. (s.f.). Alcooli. Recuperat din: colapret.cm.utexas.edu
- Parteneriatul pentru educația în farmacologie a alcoolului. (s.f.). Ce este alcoolul? Universitatea Duke. Recuperat de la: sites.duke.edu
- Whittemore F. (s.f.). Tipuri și utilizări de alcool. Recuperat de pe: livestrong.com
- Wikipedia. (2018). Alcool. Recuperat de pe: en.wikipedia.org


Nimeni nu a comentat acest articol încă.