
Structura, proprietățile, producția, utilizările fosfatului de aluminiu (AlPO4)

fosfat de aluminiu este un solid anorganic format dintr-un ion de aluminiu Al3+ și un ion fosfat PO43-. Formula sa chimică este AlPO4. Este un solid alb a cărui structură cristalină este similară cu cea a siliciului SiODouă. Este insolubil în apă.
Poate fi obținut din alumină (AlDouăSAU3) și acid fosforic (H3PO4). De asemenea, poate fi obținut pornind de la soluții apoase de clorură de aluminiu (AlCl3) și fosfat de sodiu (Na3PO4).

Fosfatul de aluminiu are un punct de topire foarte ridicat, motiv pentru care este utilizat pe scară largă ca componentă a ceramicii refractare, adică a ceramicii care rezistă la temperaturi foarte ridicate..
Este, de asemenea, utilizat ca antiacid pentru stomac, în amestecuri pentru repararea dinților și ca adjuvant la vaccinuri, adică pentru a stimula răspunsul imun al organismului.
Unele betoane refractare au AlPO4 în compoziția sa, ceea ce mărește proprietățile mecanice și de susținere a temperaturii ridicate ale acestui tip de ciment.
A fost folosit ca scut de protecție pentru a preveni arderea materialelor combustibile, cum ar fi anumiți polimeri.
Indice articol
- 1 Structură
- 2 Nomenclatură
- 3 Proprietăți
- 3.1 Starea fizică
- 3.2 Greutate moleculară
- 3.3 Punctul de topire
- 3.4 Densitatea
- 3.5 Solubilitate
- 3.6 Alte proprietăți
- 4 Obținerea
- 5 Utilizare în ceramică
- 5.1 Fabricarea ceramicii cu fosfat de aluminiu
- 6 Alte utilizări
- 6.1 În obținerea betonului
- 6.2 În cimenturile dentare
- 6.3 În vaccinuri
- 6.4 Ca ignifug în polimeri
- 7 Referințe
Structura
AlPO4 Este format dintr-un cation de aluminiu Al3+ și un anion fosfat PO43-.
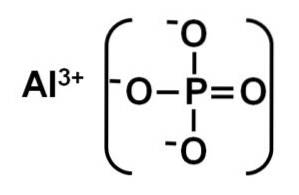
Fosfatul de aluminiu cristalin se mai numește faza berlinită sau alfa (α-AlPO4) și cristalele sale sunt similare cuarțului.

Faza alfa a fosfatului de aluminiu este un solid format dintr-o rețea covalentă de tetraedre PO4 și AlPO4 care alternează și sunt legate de atomii de oxigen.
Această structură este izomorfă cu silice, adică are aceeași formă cu cea a siliciului SiODouă.
Nomenclatură
- Fosfat de aluminiu
- Monofosfat de aluminiu
- Sare de aluminiu a acidului fosforic.
Proprietăți
Starea fizică
Cristal alb solid.
Greutate moleculară
121,93 g / mol
Punct de topire
1800 ºC
Densitate
2,56 g / cm3
Solubilitate
Insolubil în apă
Alte proprietăți
Structura AlPO4 este foarte asemănător cu siliciul SiODouă, deci împărtășește multe proprietăți fizice și chimice ale acestuia.
Fosfatul de aluminiu este un material foarte refractar, adică rezistă la temperaturi foarte ridicate fără a-și schimba starea fizică sau structura și fără a se descompune.
AlPO4 cristalin sau berlinit atunci când este încălzit se transformă într-o structură de tip tridimit și apoi de tip cristobalit, alte forme ale acestui compus care seamănă cu silica SiODouă.

Obținerea
Fosfat de aluminiu AlPO4 poate fi obținut prin reacția dintre acidul fosforic H3PO4 și alumina AlDouăSAU3. Este necesară aplicarea temperaturii, de exemplu între 100 și 150 ° C.
PentruDouăSAU3 + 2 ore3PO4 = 2 AlPO4 + 3 HDouăSAU
Poate fi obținut și prin îmbinarea unei soluții apoase de clorură de aluminiu AlCl3 cu o soluție apoasă de fosfat de sodiu Na3PO4:
AlCl3 + N / A3PO4 = AlPO4 + 3 NaCI
Utilizare în ceramică
Fosfat de aluminiu AlPO4 se găsește adesea în constituția ceramicii de alumină.
Ceramica cu conținut ridicat de alumină este unul dintre materialele care, datorită durității sale, este utilizat în aplicații în care este necesar să reziste la sarcini mari și condiții severe..
Acest tip de ceramică este rezistent la coroziune, la medii cu temperaturi ridicate, la prezența aburului fierbinte sau la atmosfere reducătoare precum monoxidul de carbon (CO)..
Ceramica cu alumină are, de asemenea, o conductivitate electrică și termică scăzută, motiv pentru care este utilizată la fabricarea cărămizilor refractare și a componentelor izolatoare electric..

Deoarece fosfatul de aluminiu se formează la o temperatură mult mai scăzută decât siliciul SiODouă, producția sa este mai ieftină, ceea ce constituie un avantaj în fabricarea ceramicii potrivite pentru servicii solicitante.
Fabricarea ceramicii de fosfat de aluminiu
Se folosește aluminăDouăSAU3 și acid fosforic H3PO4 în mediu apos.
PH-ul de formare preferat este 2-8, deoarece există o abundență de specii de acid fosforic dizolvat, cum ar fi HDouăPO4- și HPO4Două-. La pH acid concentrația ionilor de Al3+ este ridicat, provenind din dizolvarea aluminei AlDouăSAU3.
Mai întâi, se formează un gel AlH de difosfat de aluminiu trihidrogen hidratat.3(PO4)Două.HDouăSAU:
Pentru3+ + HDouăPO4- + HPO4Două- + HDouăO ⇔ AlH3(PO4)3.HDouăSAU
Cu toate acestea, vine un moment în care pH-ul soluției scade și devine neutru, unde alumina AlDouăSAU3 are o solubilitate redusă. În acest moment, alumina insolubilă formează un strat pe suprafața particulelor, împiedicând reacția să continue..
Prin urmare, este necesar să se mărească solubilitatea aluminei și acest lucru se realizează prin încălzirea ușoară. La încălzire la 150 ° C gelul continuă reacția cu alumina AlDouăSAU3 eliberând apă și berlinită cristalină (alfa-AlPO4).
PentruDouăSAU3 + 2 AlH3(PO4)3.HDouăO → AlPO4 + 4 oreDouăSAU
Berlinita leagă particulele individuale și formează ceramica.
Alte utilizări
AlPO4 Este utilizat ca antiacid, ca adsorbant, ca sită moleculară, ca suport catalizator și ca strat de acoperire pentru a îmbunătăți rezistența la coroziune la cald. Sub alte aplicații.
În obținerea betonului
Fosfatul de aluminiu este un ingredient din betoanele refractare sau betoanele rezistente la căldură.
Oferă proprietăți mecanice și refracționale excelente acestor betoane, cum ar fi rezistența la căldură. În intervalul de temperatură cuprins între 1400-1600 ° C, betonul celular pe bază de fosfat de aluminiu este unul dintre cele mai eficiente materiale ca izolator termic..
Nu necesită uscare, întărirea sa se realizează printr-o reacție exotermă de auto-propagare. Este posibil să se pregătească cărămizi din acest material de orice formă și dimensiune.
În cimenturile dentare
Fosfatul de aluminiu face parte din cimenturile dentare sau din materialele utilizate pentru vindecarea dinților deteriorați.
În cimenturile dentare, alumina este utilizată ca moderator al reacțiilor acid-bazice, unde efectul de moderare se datorează formării fosfatului de aluminiu asupra particulelor altor materiale..
Aceste cimenturi au o rezistență foarte mare la compresiune și tensiune, care se datorează prezenței fosfatului de aluminiu.
În vaccinuri
AlPO4 A fost folosit de mulți ani în diferite vaccinuri umane pentru a spori răspunsul imun al organismului. Se spune că AlPO4 este un „adjuvant” pentru vaccinuri. Mecanismul nu este încă bine înțeles.
Se știe că efectul imunostimulator al AlPO4 depinde de procesul de adsorbție a antigenului la adjuvant, adică de modul în care acesta aderă la acesta. Un antigen este un compus care la intrarea în organism generează formarea de anticorpi pentru combaterea unei boli specifice.
Antigenii pot fi adsorbiți la AlPO4 prin interacțiuni electrostatice sau prin legarea cu liganzi. Acestea sunt adsorbite pe suprafața adjuvantului.
Se crede, de asemenea, că dimensiunea particulelor de AlPO4 are și influență. Cu cât dimensiunea particulelor este mai mică, răspunsul anticorpului este mai mare și durează mai mult..
Ca ignifug în polimeri
AlPO4 A fost folosit ca un agent ignifug și pentru a preveni arderea sau arderea anumitor polimeri.
Adăugarea AlPO4 la un polimer de polipropilenă care are deja un ignifug cauzează un efect sinergic între ambii agenți de întârziere, ceea ce înseamnă că efectul este mult mai mare decât cel al ambilor ignifugi separat.
Când polimerul este supus arderii sau ars în prezența AlPO4, se formează un metafosfat de aluminiu care pătrunde în suprafața carbonizată și umple porii și fisurile acestuia.
Acest lucru duce la formarea unui scut protector extrem de eficient pentru a preveni arderea sau arderea polimerului. Cu alte cuvinte, AlPO4 sigilează suprafața carbonizată și previne arderea polimerului.

Referințe
- Abyzov, V.A. (2016). Beton refractar ușor pe bază de liant aluminiu-magneziu-fosfat. Procedia Engineering 150 (2016) 1440-1445. Recuperat de la sciencedirect.com.
- Wagh, A.S. (2016). Ceramică cu fosfat de aluminiu. În ceramică fosfat legat chimic (ediția a doua). Capitolul 11. Recuperat de la sciencedirect.com.
- Mei, C. și colab. (2019). Adjuvant pentru vaccinul cu fosfat de aluminiu: analiza compoziției și dimensiunii utilizând instrumente off-line și in-line. Comput Struct Biotechnol J. 2019; 17: 1184-1194. Recuperat de la ncbi.nlm.nih.gov.
- Qin, Z. și colab. (2019). Efectul barierei sinergice al fosfatului de aluminiu asupra polipropilenei ignifuge pe baza sistemului polifosfat de amoniu / dipentaeritritol. Materiale și proiectare 181 (2019) 107913. Recuperat de la sciencedirect.com.
- Vrieling, H. și colab. (2019). Nanoparticule de aluminiu fosfat stabilizat utilizate ca adjuvant pentru vaccin. Coloizi și suprafețe B: interfețe bio 181 (2019) 648-656. Recuperat de la sciencedirect.com.
- Schaefer, C. (2007). Medicamente gastrointestinale. Antiacide. În medicamente în timpul sarcinii și alăptării (ediția a doua). Recuperat de la sciencedirect.com.
- .


Nimeni nu a comentat acest articol încă.