
Caracteristici, structură, funcții ale mucoasei
fucose (prescurtat Fuc), sau 6-L-deoxi-galactoză, este o monozaharidă cu șase carbon parțial dezoxigenată (deoxisugar) a cărei formulă empirică este C6H12SAU5. La fel ca alte monozaharide, este un zahăr polihidric.
Când o grupare hidroxil este înlocuită cu un atom de hidrogen, se derivă un deoxisugar. Deși teoretic această înlocuire ar putea afecta orice grupare hidroxil a oricărui monozaharid, în natură există o varietate redusă de deoxisugari.
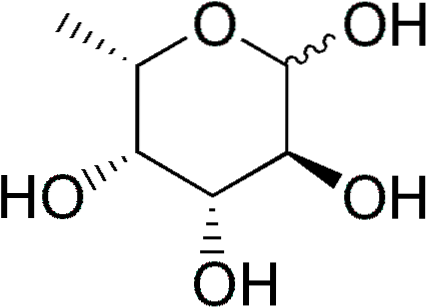
Unele deoxisugare sunt: 1) dezoxiriboză (2-deoxi-D-riboză), derivată din D-riboză, care face parte din ADN; 2) ramnoză (6-D-dezoximanoză), derivată din D-manoză; 3) fucoză, derivată din L-galactoză. Aceasta din urmă este mai frecventă decât D-fucoză, derivată din D-galactoză.
Indice articol
- 1 Caracteristici și structură
- 2 Distribuție în natură
- 3 Metabolismul glucozei
- 4 Funcții
- 4.1 Rolul în cancer
- 4.2 Rolul în alte boli
- 4.3 Potențial biomedical
- 5 Referințe
Caracteristici și structură
Fucoza este cunoscută și sub denumirea de 6-deoxi-galacto-hexoză, fucopiranoză, galactometiloză și rodoză..
Deși se găsește în mod normal în formarea polizaharidelor și glicoproteinelor, izolată ca monozaharidă, este mai dulce decât galactoza. Acest lucru se datorează faptului că înlocuirea unei grupări hidroxil cu un atom de hidrogen crește caracterul hidrofob și, prin urmare, dulceața moleculei..
Grupurile hidroxil de fucoză pot suferi aceleași reacții ca și alte zaharuri, producând o mare varietate de acetali, glicozide, eteri și esteri..
O biomoleculă fucosilată este una la care, prin acțiunea unei fucosiltransferaze, moleculele de fucoză au fost atașate prin legături glicozidice. Când hidroliza legăturilor glicozidice are loc prin acțiunea unei fucozidaze, separând astfel fucoza, se spune că biomolecula a fost defucozilată.
Când glucanii sunt fucosilați, se generează glucani mai complecși numiți fucani, care pot sau nu să facă parte din glicoproteine. Fucanii sulfați sunt definiți ca acele polizaharide care conțin reziduuri sulfatate de L-fucoză. Sunt tipice algelor brune. Exemplele includ ascofilan, sargasan și pelvetan..
Unul dintre cei mai bine studiați fucani este fucoidanul, obținut din alge brune Fucus vesiculosus, care a fost comercializat (Sigma-Aldrich Chemical Company) de zeci de ani.
Distribuție în natură
D-fucoza este prezentă în substanțele antibiotice produse de microbi și în glicozidele plantelor, cum ar fi convolvulina, chartreusina, ledienozida și keirotoxina.
L-fucoza este un constituent al polizaharidelor din alge, frunze de prune, in, semințe de soia și canola, tragacant gumă, pereți celulari de cartofi, tuberculi de manioc, fructe de kiwi, scoarța ceiba și mucigelul porumbului caliptra, precum și alte plante.
L-fucoza este prezentă și în ouăle de arici și în gelatina care protejează ouăle de broască.
La mamifere, fucanii cu L-fucoză formează liganzii care acționează asupra adeziunii leucocite-endoteliale mediate de selectină și participă la numeroase evenimente ontogenetice.
L-fucoza este abundentă în fucosfingolipidele epiteliului gastro-intestinal și măduvei osoase și apare în proporții mici în cartilaj și structuri keratinoase.
La om, fucanii L-fucoză fac parte din glicoproteinele din salivă și sucurile gastrice. Acestea fac, de asemenea, parte din antigenele care definesc grupele sanguine ABO. Sunt prezente în diferite oligozaharide din laptele matern.
Metabolismul glucozei
Fucosiltransferazele utilizează GDP-fucoză, o formă de fucoză activată cu nucleotide, ca donator de fucoză în construcția oligozaharidelor fucozilate.
PIB-fucoza este derivată din PIB-manoză prin acțiunea succesivă a două enzime: PIB-manoză 4,6-dehidratază și PIB-4-ceto-6-deoximanoză 3,5-epimerază-4-reductază.
Folosind un cofactor NADP +, prima enzimă catalizează deshidratarea PIB-manozei. Reducerea poziției 6 și oxidarea poziției 4 produce PIB-6-deoxi-4-ceto-manoză (în timpul reacției, hibridul este transferat din poziția 4 la 6 a zahărului).
A doua enzimă, care este dependentă de NADPH, catalizează epimerizarea pozițiilor 3 și 5 și reducerea grupării 4-ceto, a GDP-6-deoxi-4-ceto-manoză..
Bacteriile pot crește folosind fucoza ca singură sursă de carbon și energie prin intermediul unui operon inducibil de fucoză care codifică enzimele catabolice pentru acest zahăr..
Procesul de mai sus implică: 1) intrarea fucozei libere prin peretele celular mediat de o permează; 2) izomerizarea fucozei (o aldoză) pentru a forma fuculoza (o cetoză); 3) fosforilarea fuculozei pentru a forma fuculoza-1-fosfat; 4) o reacție aldolazică pentru a forma lactaldehidă și dihidroxiacetonă fosfat din fuculoză-1-fosfat.
Caracteristici
Rolul în cancer
Simptomele multor tipuri de tumori canceroase includ prezența proteinelor legate de glucan care se disting prin prezența unei compoziții oligozaharidice modificate. Prezența acestor glucani anormali, printre care se remarcă fucanii, este legată de malignitatea și potențialul metastatic al acestor tumori.
În cancerul de sân, celulele tumorale încorporează fucoza în glicoproteine și glicolipide. Fucoza contribuie la progresia acestui cancer, favorizând activarea celulelor stem canceroase, metastaza hematogenă și invazia tumorilor prin matrici extracelulare.
În carcinomul pulmonar și hepatocarcinogeneza, expresia crescută a fucozei este asociată cu un potențial metastatic ridicat și o probabilitate scăzută de supraviețuire.
În schimb, unii fucani sulfatați sunt substanțe promițătoare în tratamentul cancerului, așa cum a fost determinat de numeroase studii in vitro cu linii celulare canceroase, inclusiv cele care cauzează cancer de sân, plămâni, prostată, gastric, de colon și rect..
Rolul în alte boli
Expresia crescută a fucanilor în imunoglobulinele serice a fost asociată cu artrita reumatoidă juvenilă și adultă.
Deficitul de adeziune leucocitară II este o boală congenitală rară datorată mutațiilor care modifică activitatea unui transportor FDP-fucoză situat în aparatul Golgi.
Pacienții suferă de întârziere mentală și psihomotorie și suferă de infecții bacteriene recurente. Această boală răspunde favorabil la dozele orale de fucoză.
Potențial biomedical
Fucanii sulfați obținuți din algele brune sunt rezervoare importante de compuși cu potențial terapeutic.
Au proprietăți antiinflamatorii și antioxidante, inhibând migrația limfocitelor în locurile de infecție și favorizând eliberarea citokinelor. Creșteți răspunsul imun prin activarea limfocitelor și macrofagelor.
Au proprietăți anticoagulante. S-a demonstrat oral că inhibă agregarea plachetară la pacienții umani.
Au potențial antibiotic și antiparazitar și inhibă dezvoltarea bacteriilor patogene din stomac Helicobacter pylori. Ucideți paraziții Plasmodium spp. (agent cauzal al malariei) și Leishmania donovani (agent cauzal al leishmaniozei viscerotrope americane).
În cele din urmă, acestea au proprietăți antivirale puternice, inhibând intrarea în celulă a mai multor viruși de mare importanță pentru sănătatea umană, inclusiv Arenavirus, Citomegalovirus, Hantavirus, Hepadnavirus, HIV, virusul herpes simplex și virusul gripal.
Referințe
- Becker, D. J., Lowe, J. B. 2003. Fucoza: biosinteza și funcția biologică la mamifere. Glicobiologie, 13, 41R-53R.
- Deniaud-Bouët, E., Hardouin, K., Potin, P., Kloareg, B., Hervé, C. 2017. O recenzie despre pereții celulelor de algă maro și polizaharidele sulfatate care conțin fucoză: contextul peretelui celular, proprietăți biomedicale și cheie provocări de cercetare Polimeri carbohidrați, http://dx.doi.org/10.1016/j.carbpol.2017.07.082.
- Flowers H. M. 1981. Chimia și biochimia D- și L-fucozei. Progrese în chimia și biochimia carbohidraților, 39, 279-345.
- Listinsky, J. J., Siegal, G. P., Listinsky, C. M. 2011. Importanța emergentă a α-L-fucoza în cancerul de sân uman: o recenzie. Am. J. Transl. Rez., 3, 292-322.
- Murray, R. K., și colab. 2003. Biochimia ilustrată a lui Harper. McGraw-Hill, New York.
- Pereira, L. 2018. Utilizări terapeutice și nutriționale ale algelor. CRC Press, Boca Raton.
- Staudacher, E., Altmann, F., Wilson, I. B. H., März, L. 1999. Fucoza în N-glicani: de la plantă la om. Biochimica și Biophysica Acta, 1473, 216-236.
- Tanner, W., Loewus, F. A. 1981. Glucide vegetale II. Glucide extracelulare. Springer, New York.
- Vanhooren, P. T., Vandamme, E. J. 1999. L-fucoză: apariție, rol fiziologic, sinteză chimică, enzimatică și microbiană. Jurnalul de tehnologie chimică și biotehnologie, 74, 479-497.


Nimeni nu a comentat acest articol încă.