
Proprietăți și exemple de hidrocarburi nesaturate

hidrocarburi nesaturate sunt cele care conțin cel puțin o legătură dublă de carbon în structura lor, fiind capabil să conțină o legătură triplă, deoarece saturația unui lanț înseamnă că a primit toți atomii de hidrogen posibili în fiecare carbon și nu există perechi de electroni liberi unde pot intra mai mulți hidrogeni.
Hidrocarburile nesaturate sunt împărțite în două tipuri: alchene și alchine. Alchenele sunt compuși de hidrocarburi care au una sau mai multe legături duble în molecula lor. Între timp, alchinele sunt compuși de hidrocarburi care au una sau mai multe legături triple în formula lor..
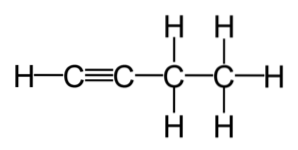
Alchenele și alchinele sunt frecvent utilizate comercial. Aceștia sunt compuși cu un nivel de reactivitate mai mare decât cel al hidrocarburilor saturate, ceea ce le face punctul de plecare al multor reacții, generate din cele mai comune alchene și alchine..
Indice articol
- 1 Nomenclatură
- 1.1 Nomenclatura alchenelor
- 1.2 Nomenclatura alchinelor
- 2 Proprietăți
- 2.1 Legături duble și triple
- 2.2 izomerizarea cis-trans
- 2.3 Aciditate
- 2.4 Polaritate
- 2.5 Puncte de fierbere și topire
- 3 Exemple
- 3.1 Etilenă (C2H4)
- 3.2 Etină (C2H2)
- 3.3 Propilena (C3H6)
- 3.4 Ciclopenten (C5H8)
- 4 Articole de interes
- 5 Referințe
Nomenclatură
Hidrocarburile nesaturate sunt denumite diferit în funcție de faptul că sunt alchene sau alchine, folosind sufixele „-eno” și „-ino”.
Alchenele au cel puțin o legătură dublă carbon-carbon în structura lor și au formula generală CnH2n, în timp ce alchinele conțin cel puțin o legătură triplă și sunt tratate cu formula CnH2n-2.
Nomenclatura alchenelor
Pentru a denumi alchenele, trebuie indicate pozițiile dublei legături carbon-carbon. Numele compușilor chimici care conțin legături C = C se termină cu sufixul „-eno”.
Ca și în cazul alcanilor, denumirea compusului de bază este determinată de numărul de atomi de carbon din cel mai lung lanț. De exemplu, molecula CHDouă= CH-CHDouă-CH3 se va numi „1-butenă”, dar cea a lui H3C-CH = CH-CH3 se va numi „2-butenă”.
Numerele observate în numele acestor compuși indică atomul de carbon cu cel mai mic număr din lanțul în care se află legătura C = C a alchenei..
Numărul de carboni din acest lanț identifică prefixul numelui, similar cu alcanii („met-”, „et-”, „pro-”, „but-” etc.), dar folosind întotdeauna sufixul „-eno ".
De asemenea, trebuie specificat dacă molecula este cis sau trans, care sunt tipuri de izomeri geometrici. Aceasta este adăugată în nume, cum ar fi 3-etil-cis-2-heptan sau 3-etil-trans-2-heptan.
Nomenclatura alchinelor
Pentru a ghici numele compușilor chimici care conțin legături triple C≡C, numele compusului este determinat de numărul de atomi de C din cel mai lung lanț.
Similar cu cazul alchenelor, numele alchinelor indică poziția în care se găsește tripla legătură carbon-carbon; de exemplu, în cazurile de HC≡C-CHDouă-CH3, sau „1-butin” și H3C-C≡C-CH3, sau „2-butin”.
Proprietăți
Hidrocarburile nesaturate cuprind un număr enorm de molecule diferite, motiv pentru care prezintă o serie de caracteristici care le definesc, care sunt identificate mai jos:
Legături duble și triple
Legăturile duble și triple ale alchenelor și alchinelor au caracteristici speciale care le diferențiază de legăturile simple: o legătură simplă reprezintă cea mai slabă dintre cele trei, fiind formată dintr-o legătură sigma între două molecule..
Legătura dublă este formată dintr-o legătură sigma și un pi, iar legătura triplă de o legătură sigma și doi pi. Acest lucru face alchenele și alchinele mai puternice și necesită mai multă energie pentru a se descompune atunci când apar reacții..
În plus, unghiurile de legătură care se formează într-o legătură dublă sunt de 120 °, în timp ce cele ale legăturii triple sunt de 180 °. Aceasta înseamnă că moleculele cu legături triple au un unghi liniar între acești doi atomi de carbon..
Izomerizarea Cis-trans
La alchene și alți compuși cu duble legături, are loc o izomerizare geometrică, care diferă de partea legăturilor în care se găsesc grupările funcționale care sunt atașate la carbonii implicați în această dublă legătură..
Când grupările funcționale ale unei alchene sunt orientate în aceeași direcție în raport cu legătura dublă, această moleculă este denumită cis, dar când substituenții sunt în direcții diferite, se numește trans.
Această izomerizare nu este o simplă diferență de localizare; compușii pot varia foarte mult doar pentru că sunt geometrie cis sau geometrie trans.
Compușii Cis implică de obicei forțe dipol-dipol (care au o valoare netă de zero în trans); În plus, au o polaritate mai mare, puncte de fierbere și topire și sunt de densitate mai mare decât omologii lor trans. În plus, compușii trans sunt mai stabili și eliberează mai puțină căldură de ardere..
Aciditate
Alchenele și alchinele au o aciditate mai mare în comparație cu alcanii, datorită polarității legăturilor lor duble și triple. Sunt mai puțin acizi decât alcoolii și acizii carboxilici; iar dintre cele două, alchinele sunt mai acide decât alchenele.
Polaritate
Polaritatea alchenelor și a alchinelor este scăzută, cu atât mai mult în compușii transalcheni, ceea ce face ca acești compuși să fie insolubili în apă..
Totuși, hidrocarburile nesaturate se dizolvă ușor în solvenți organici obișnuiți, cum ar fi eteri, benzen, tetraclorură de carbon și alți compuși cu polaritate scăzută sau fără polaritate..
Puncte de fierbere și topire
Datorită polarității lor scăzute, punctele de fierbere și topire ale hidrocarburilor nesaturate sunt scăzute, aproape echivalente cu cele ale alcanilor care au aceeași structură de carbon..
Chiar și așa, alchenele au puncte de fierbere și de topire mai scăzute decât alcanii corespunzători, putând scădea și mai mult dacă sunt izomerici cis, așa cum sa menționat anterior..
În schimb, alchinele au puncte de fierbere și topire mai mari decât alcanii și alchenele corespunzătoare, deși diferența este de doar câteva grade..
În cele din urmă, cicloalcenele au, de asemenea, temperaturi de topire mai scăzute decât cicloalcanii corespunzători, datorită rigidității legăturii duble..
Exemple
Etilenă (CDouăH4)
Un compus chimic puternic datorită capacității sale de polimerizare, oxidare și halogenare, printre alte caracteristici.
Ethyne (C.DouăHDouă)
Numit și acetilenă, este un gaz inflamabil care este folosit ca sursă utilă de iluminare și căldură..
Propilenă (C3H6)
Al doilea compus cel mai utilizat în industria chimică la nivel mondial, este unul dintre produsele termolizei petrolului.
Ciclopenten (C5H8)
Un compus de tip cicloalchen. Această substanță este utilizată ca monomer pentru sinteza materialelor plastice.
Articole de interes
Hidrocarburi saturate sau alcani.
Referințe
- Chang, R. (2007). Chimie, ediția a IX-a. Mexic: McGraw-Hill.
- Wikipedia. (s.f.). Alchene. Adus de pe en.wikipedia.org
- Boudreaux, K. A. (s.f.). Hidrocarburi nesaturate. Adus de la angelo.edu
- Tuckerman, M. E. (s.f.). Alchene și Alchine. Adus de la nyu.edu
- Universitatea, L. T. (s.f.). Hidrocarburile nesaturate: alchene și alchine. Adus de la chem.latech.edu



Nimeni nu a comentat acest articol încă.