
Descoperirea razelor anodice, proprietăți

raze anodice sau raze canal, De asemenea, numite pozitive, acestea sunt fascicule de raze pozitive formate din cationi atomici sau moleculari (ioni încărcați pozitiv) care sunt direcționați către electrodul negativ dintr-un tub Crookes.
Razele anodice își au originea atunci când electronii care merg de la catod spre anod, ciocnesc cu atomii gazului închis în tubul Crookes.

Pe măsură ce particulele cu același semn se resping reciproc, electronii care merg spre anod distrug electronii prezenți în scoarța atomilor de gaz..
Astfel, atomii care au rămas încărcați pozitiv - adică au fost transformați în ioni pozitivi (cationi) - sunt atrași de catod (încărcați negativ).
Indice articol
- 1 Descoperire
- 2 Proprietăți
- 3 Un pic de istorie
- 3.1 Tubul de raze anodice
- 3.2 Protonul
- 3.3 Spectrometrie de masă
- 4 Referințe
Descoperire
Fizicianul german Eugen Goldstein a fost cel care le-a descoperit, observându-le pentru prima dată în 1886.
Ulterior, munca efectuată pe razele anodice de către oamenii de știință Wilhelm Wien și Joseph John Thomson a ajuns să presupună dezvoltarea spectrometriei de masă.
Proprietăți
Principalele proprietăți ale razelor anodice sunt următoarele:
- Au o sarcină pozitivă, valoarea sarcinii lor fiind un multiplu întreg al sarcinii electronului (1,6 ∙ 10-19 C).
- Se mișcă în linie dreaptă în absența câmpurilor electrice și a câmpurilor magnetice.
- Acestea deviază în prezența câmpurilor electrice și a câmpurilor magnetice, deplasându-se spre zona negativă.
- Poate pătrunde în straturi subțiri de metale.
- Pot ioniza gaze.
- Atât masa, cât și sarcina particulelor care alcătuiesc razele anodice variază în funcție de gazul închis în tub. În mod normal, masa lor este identică cu masa atomilor sau moleculelor din care sunt derivați..
- Ele pot provoca modificări fizice și chimice.
Puțină istorie
Înainte de descoperirea razelor anodice, a avut loc descoperirea razelor catodice, care a avut loc de-a lungul anilor 1858 și 1859. Descoperirea se datorează lui Julius Plücker, matematician și fizician de origine germană..
Mai târziu, fizicianul englez Joseph John Thomson a studiat în profunzime comportamentul, caracteristicile și efectele razelor catodice.
La rândul său, Eugen Goldstein - care efectuase anterior alte investigații cu raze catodice - a fost cel care a descoperit razele anodice. Descoperirea a avut loc în 1886 și a făcut-o când și-a dat seama că tuburile de descărcare cu catodul perforat emit și lumină la capătul catodului..
În acest fel a descoperit că, pe lângă razele catodice, existau și alte raze: razele anodice; acestea se deplasau în direcția opusă. Deoarece aceste raze treceau prin găurile sau canalele din catod, el a decis să le numească raze de canal..
Cu toate acestea, nu el, ci Wilhelm Wien a făcut ulterior studii ample asupra razelor anodice. Wien, împreună cu Joseph John Thomson, au ajuns să stabilească baza spectrometriei de masă.
Descoperirea lui Eugen Goldstein despre razele anodice a constituit un pilon fundamental pentru dezvoltarea ulterioară a fizicii contemporane..
Datorită descoperirii razelor anodice, roiuri de atomi în mișcare rapidă și ordonată au devenit disponibile pentru prima dată, a căror aplicare a fost foarte fertilă pentru diferite ramuri ale fizicii atomice..
Tubul cu raze anodice
În descoperirea razelor anodice, Goldstein a folosit un tub de descărcare care avea catodul perforat. Procesul detaliat prin care se formează razele anodice într-un tub de evacuare a gazului este următorul.
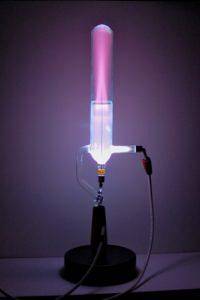
Prin aplicarea unei diferențe mari de potențial de câteva mii de volți tubului, câmpul electric care se creează accelerează numărul mic de ioni care sunt întotdeauna prezenți într-un gaz și care sunt creați prin procese naturale precum radioactivitatea..
Acești ioni accelerați se ciocnesc cu atomii din gaz, smulgând electroni din ei și creând ioni mai pozitivi. La rândul lor, acești ioni și electroni atacă din nou mai mulți atomi, creând ioni mai pozitivi în ceea ce este o reacție în lanț..
Ionii pozitivi sunt atrași de catodul negativ și unii trec prin găurile din catod. Până ajung la catod, au accelerat deja suficient de repede încât, atunci când se ciocnesc cu alți atomi și molecule din gaz, excită specia la niveluri de energie mai ridicate..
Când aceste specii revin la nivelurile lor originale de energie, atomii și moleculele eliberează energia pe care o câștigaseră anterior; energia este emisă sub formă de lumină.
Acest proces de producție a luminii, numit fluorescență, face să apară o strălucire în regiunea în care ionii ies din catod.
Protonul
Deși Goldstein a obținut protoni cu experimentele sale cu raze anodice, adevărul este că nu el este cel care este creditat cu descoperirea protonului, deoarece nu a putut să-l identifice corect.
Protonul este cea mai ușoară dintre particulele pozitive produse în tuburile cu raze anodice. Protonul este produs atunci când tubul este încărcat cu hidrogen gazos. În acest fel, atunci când hidrogenul se ionizează și își pierde electronul, se obțin protoni..
Protonul are o masă de 1,67 ∙ 10-24 g, aproape la fel ca cea a atomului de hidrogen și are aceeași sarcină, dar cu semnul opus ca cea a electronului; adică 1,6 ∙ 10-19 C.
Spectrometrie de masa
Spectrometria de masă, dezvoltată din descoperirea razelor anodice, este o procedură analitică care permite studierea compoziției chimice a moleculelor unei substanțe pe baza masei acestora..
Permite atât recunoașterii compușilor necunoscuți, numărării compușilor cunoscuți, cât și cunoașterii proprietăților și structurii moleculelor unei substanțe.
La rândul său, spectrometrul de masă este un dispozitiv cu ajutorul căruia structura diferiților compuși chimici și izotopi poate fi analizată într-un mod foarte precis..
Spectrometrul de masă permite separarea nucleelor atomice pe baza relației dintre masă și sarcină.

Referințe
-
- Raza anodică (n.d.). Pe Wikipedia. Adus pe 19 aprilie 2018, de pe es.wikipedia.org.
- Raza anodică (n.d.). Pe Wikipedia. Adus pe 19 aprilie 2018, de pe en.wikipedia.org.
- Spectrometru de masă (n.d.). Pe Wikipedia. Adus pe 19 aprilie 2018, de pe es.wikipedia.org.
- Grayson, Michael A. (2002). Măsurarea masei: de la raze pozitive la proteine. Philadelphia: Chemical Heritage Press
- Grayson, Michael A. (2002). Măsurarea masei: de la raze pozitive la proteine. Philadelphia: Chemical Heritage Press.
- Thomson, J. J. (1921). Raze de electricitate pozitivă și aplicarea lor la analizele chimice (1921)
- Fidalgo Sánchez, José Antonio (2005). Fizică și chimie. Everest



Nimeni nu a comentat acest articol încă.