
Săruri de diazoniu Formare, proprietăți și aplicații
săruri de diazoniu sunt compuși organici în care există interacțiuni ionice între grupul azo (-NDouă+) și un anion X- (Cl-, F-, CH3GÂNGURI-, etc.). Formula sa chimică generală este RNDouă+X-, și în aceasta, lanțul lateral R poate fi o grupare alifatică sau o grupare arii; adică un inel aromatic.
Imaginea inferioară reprezintă structura ionului arenediazoniu. Sferele albastre corespund grupului azo, în timp ce sferele alb-negru alcătuiesc inelul aromatic al grupării fenil. Grupa azo este foarte instabilă și reactivă, deoarece unul dintre atomii de azot are o sarcină pozitivă (-N+≡N).
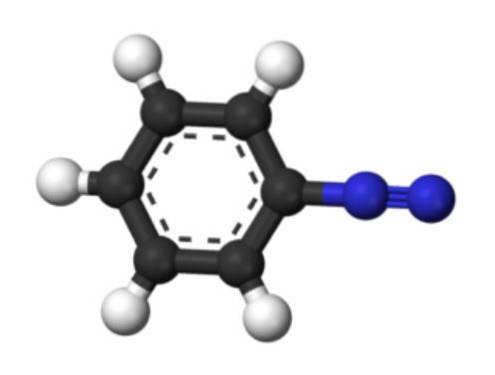
Cu toate acestea, există structuri de rezonanță care delocalizează această sarcină pozitivă, de exemplu, pe atomul de azot vecin: -N = N+. Acest lucru apare atunci când o pereche de electroni care formează o legătură se îndreaptă către atomul de azot din stânga.
La fel, această sarcină pozitivă poate fi delocalizată de sistemul Pi al inelului aromatic. În consecință, sărurile aromatice de diazoniu sunt mai stabile decât cele alifatice, deoarece sarcina pozitivă nu poate fi delocalizată de-a lungul unui lanț de carbon (CH3, CHDouăCH3, etc.).
Indice articol
- 1 Instruire
- 2 Proprietăți
- 2.1 Reacții de deplasare
- 2.2 Alte deplasări
- 2.3 Reacții redox
- 2.4 Descompunerea fotochimică
- 2.5 Reacții de cuplare azo
- 3 Aplicații
- 4 Referințe
Instruire
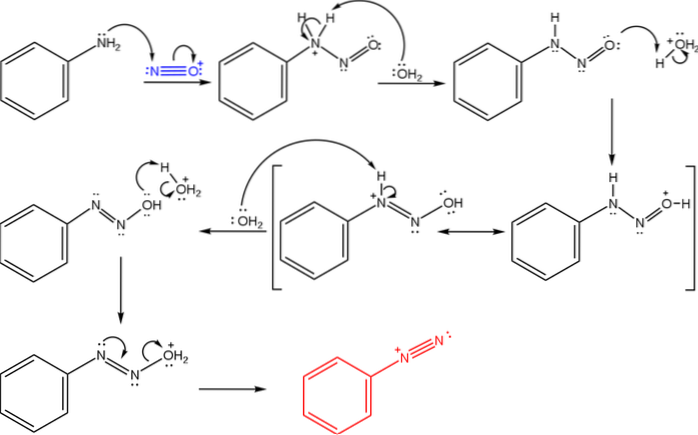
Aceste săruri sunt derivate din reacția unei amine primare cu un amestec acid de nitrit de sodiu (NaNODouă).
Amine secundare (RDouăNH) și terțiar (R3N) au originea altor produse azotate, cum ar fi N-nitrosoaminele (care sunt uleiuri gălbui), sărurile aminice (R3HN+X-) și compuși N-nitroamoniu.
Imaginea superioară ilustrează mecanismul prin care se guvernează formarea sărurilor de diazoniu sau cunoscută și sub numele de reacție de diazotizare.
Reacția începe cu fenilamină (Ar-NHDouă), care efectuează un atac nucleofil asupra atomului de N al cationului nitrosoniu (NO+). Acest cation este produs de amestecul NaNODouă/ HX, unde X este în general Cl; adică HCI.
Formarea cationului nitrosoniu eliberează apă în mediu, care elimină un proton din azotul încărcat pozitiv..
Apoi, aceeași moleculă de apă (sau o altă specie acidă, alta decât H3SAU+) cedează un proton către oxigen, delocalizând sarcina pozitivă pe atomul de azot mai puțin electronegativ).
Acum, apa deprotonează din nou azotul, producând astfel molecula de diazohidroxid (penultima din secvență).
Deoarece mediul este acid, diazohidroxidul suferă deshidratare din grupul OH; pentru a contracara postul vacant electronic, perechea liberă de N formează legătura triplă a grupului azo.
Astfel, la sfârșitul mecanismului, clorura de benzenediazoniu (C6H5NDouă+Cl-, același cation din prima imagine).
Proprietăți
În general, sărurile de diazoniu sunt incolore și cristaline, solubile și stabile la temperaturi scăzute (mai mici de 5 ° C)..
Unele dintre aceste săruri sunt atât de sensibile la impactul mecanic încât orice manipulare fizică le-ar putea detona. În cele din urmă, reacționează cu apa pentru a forma fenoli.
Reacții de deplasare
Sărurile de diazoniu sunt potențiali eliberatori de azot molecular, a căror formare este numitorul comun în reacțiile de deplasare. În acestea, o specie X deplasează grupul azo instabil, scăpând ca NDouă(g).
Reacția Sandmeyer
ArNDouă+ + CuCl => ArCl + NDouă + Cu+
ArNDouă+ + CuCN => ArCN + NDouă + Cu+
Reacția Gatterman
ArNDouă+ + CuX => ArX + NDouă + Cu+
Spre deosebire de reacția Sandmeyer, reacția Gatterman are cupru metalic în locul halogenurii sale; adică se generează CuX in situ.
Reacția Schiemann
[ArNDouă+] BF4- => ArF + BF3 + NDouă
Reacția Schiemann se caracterizează prin descompunerea termică a fluoroboratului de benzenediazoniu.
Reacția lui Gomberg Bachmann
[ArNDouă+] Cl- + C6H6 => Ar - C6H5 + NDouă + acid clorhidric
Alte deplasări
ArNDouă+ + KI => ArI + K+ + NDouă
[ArNDouă+] Cl- + H3PODouă + HDouăO => C6H6 + NDouă + H3PO3 + acid clorhidric
ArNDouă+ + HDouăO => ArOH + NDouă + H+
ArNDouă+ + TimbruDouă => ArNODouă + NDouă + Cu+
Reacții redox
Sărurile de diazoniu pot fi reduse la arilhidrazine, folosind un amestec de SnClDouă/ Acid clorhidric:
ArNDouă+ => ArNHNHDouă
De asemenea, pot fi reduse la arilamine în reduceri mai puternice cu Zn / HCl:
ArNDouă+ => ArNHDouă + NH4Cl
Descompunerea fotochimică
[ArNDouă+] X- => ArX + NDouă
Sărurile de diazoniu sunt sensibile la descompunere prin incidența radiațiilor ultraviolete sau la lungimi de undă foarte apropiate.
Reacții de cuplare azo
ArNDouă+ + Ar'H → ArNDouăAr '+ H+
Aceste reacții sunt probabil cele mai utile și mai versatile dintre sărurile de diazoniu. Aceste săruri sunt electrofile slabe (inelul delocalizează sarcina pozitivă a grupului azo). Pentru ca aceștia să reacționeze cu compuși aromatici, atunci trebuie să fie încărcați negativ, dând astfel naștere compușilor azos..
Reacția are loc cu un randament eficient între un pH de 5 și 7. În pH acid, cuplajul este mai mic, deoarece grupa azo este protonată, ceea ce face imposibilă atacarea inelului negativ..
La fel, în pH bazic (mai mare de 10), sarea de diazoniu reacționează cu OH- pentru a produce diazohidroxid, care este relativ inert.
Structurile acestui tip de compus organic au un sistem Pi conjugat foarte stabil, ai cărui electroni absorb și emit radiații în spectrul vizibil..
În consecință, compușii azo se caracterizează prin faptul că sunt colorate. Datorită acestei proprietăți au fost numiți și coloranți azoici.
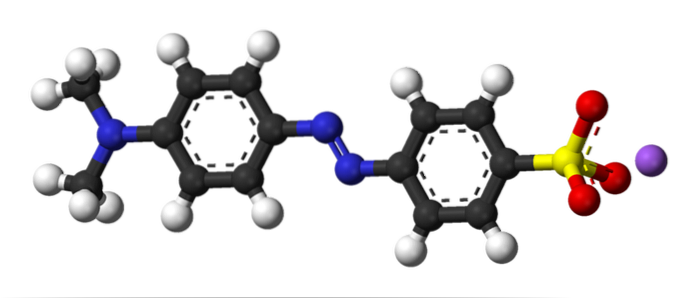
Imaginea de mai sus ilustrează conceptul de cuplare azo cu metil portocaliu ca exemplu. În mijlocul structurii sale, grupul azo poate fi văzut servind drept conector al celor două inele aromatice.
Care dintre cele două inele a fost electrofilul la începutul cuplării? Cel din dreapta, deoarece gruparea sulfonat (-SO3) elimină densitatea electronilor din inel, făcându-l și mai electrofil.
Aplicații

Una dintre aplicațiile sale cele mai comerciale este producția de coloranți și pigmenți, care cuprinde, de asemenea, industria textilă în vopsirea țesăturilor. Acești compuși azoici se ancorează pe site-uri moleculare specifice de pe polimer, colorându-l în culori.
Datorită descompunerii sale fotolitice, este (mai puțin decât înainte) utilizat în reproducerea documentelor. Cum? Suprafețele hârtiei acoperite de un plastic special sunt îndepărtate și apoi li se aplică o soluție de bază de fenol, colorând literele sau desenul albastru..
În sinteze organice sunt folosite ca puncte de plecare pentru mulți derivați aromatici.
În cele din urmă, au aplicații în domeniul materialelor inteligente. În acestea sunt legate covalent de o suprafață (aur, de exemplu), permițându-i să dea un răspuns chimic la stimulii fizici externi..
Referințe
- Wikipedia. (2018). Compus diazoniu. Adus pe 25 aprilie 2018, de pe: en.wikipedia.org
- Francis A. Carey. Chimie organica. Acizi carboxilici. (ediția a șasea, paginile 951-959). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. Chimie organica. Amine. (Ediția a X-a., Paginile 935-940). Wiley plus.
- Clark J. (2016). Reacțiile sărurilor de diazoniu. Adus la 25 aprilie 2018 de la: chemguide.co.uk
- BYJU'S. (05 octombrie 2016). Sărurile de Diazonium și aplicațiile lor. Adus pe 25 aprilie 2018 de pe: byjus.com
- TheGlobalTutors. (2008-2015). Proprietățile sărurilor de diazoniu. Adus pe 25 aprilie 2018, de pe: theglobaltutors.com
- Ahmad și colab. (2015). Polimer. Adus pe 25 aprilie 2018 de la: msc.univ-paris-diderot.fr
- CitocromT. (15 aprilie 2017). Mecanism pentru formarea ionului benzenediazoniu. Adus pe 25 aprilie 2018 de la: commons.wikimedia.org
- Jacques Kagan. (1993). Fotochimie organică: principii și aplicații. Academic Press Limited, pagina 71. Adus pe 25 aprilie 2018, de pe: books.google.co.ve



Nimeni nu a comentat acest articol încă.