
Tenecteplase pentru ce este, structura, mecanismul de acțiune, doza
tenecteplase este un activator plasminogen tisular (tPA) sintetizat de industria farmaceutică utilizând tehnici de ADN recombinant aplicate unei linii celulare obținute din celule ovariene de hamster chinezesc.
Procesul de coagulare a sângelui, care se încheie cu formarea unui tromb și retragerea cheagului, continuă cu o fază numită fibrinoliză. Această fază se caracterizează prin dizolvarea trombului prin fragmentarea polimerului de fibrină în peptide mai mici și mai solubile și recanalizarea vasului sau vaselor, unde a avut loc coagularea..
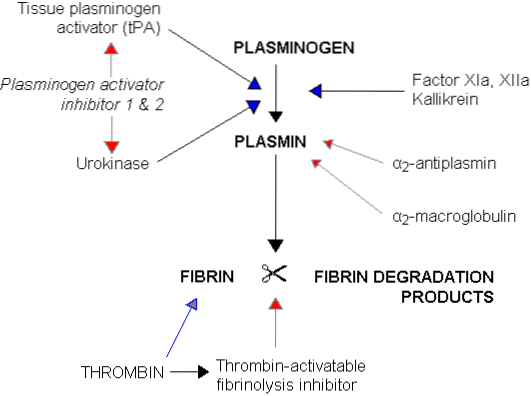
Acest proces fibrinolitic necesită participarea unei proteine din sânge din grupul de globuline plasmatice numite plasminogen sau profibrinolizină, de aproximativ 81 kDa, sintetizată în ficat și prezentă în mod normal în sângele circulant. Acest plasminogen este prins în timpul coagulării între rețelele de fibrină care alcătuiesc trombul..
Plasminogen în sine nu are nicio acțiune fibrinolitică, acțiune care apare doar atunci când molecula originală este activată și transformată în plasmină sau fibrinolizină, care este o serină protează foarte asemănătoare cu tripsina, care este cea mai importantă enzimă digestivă proteolitică din secreția pancreatică.
Plasminul are o afinitate mare pentru fibrină, pe care o descompune în mici peptide solubile care, la rândul lor, inhibă acțiunea trombinei și producția ulterioară de mai multă fibrină. De asemenea, exercită o acțiune proteolitică asupra fibrinogenului, protrombinei și factorilor de coagulare V, VIII, IX, XI și XII, ceea ce reduce și capacitatea de coagulare a sângelui.
Din acest tabel, se poate deduce că plasmina influențează procesele de coagulare a sângelui în două moduri, deoarece, pe de o parte, produce dizolvarea trombului prin acțiunea sa fibrinolitică, iar pe de altă parte, interferează cu coagularea prin acțiunea sa proteolitică. factorii procesului de coagulare.
Indice articol
- 1 Pentru ce este tenecteplase?
- 2 Structura moleculei
- 3 Mecanismul de acțiune
- 4 Prezentare
- 5 Doză
- 6 Referințe
Pentru ce este tenecteplase?
Activarea plasminogenului are loc prin acțiunea individuală sau combinată a unui set de substanțe care sunt denumite generic activatori de plasminogen și care, în funcție de originea lor, sunt grupați în activatori de plasminogen: sânge, urină, țesut și din microorganisme.
Fiind un activator plasminogen tisular care îl transformă în plasmină, iar plasmina este agentul fibrinolitic prin excelență, deoarece tenecteplaza este utilizată pentru fibrinoliza terapeutică în infarctul miocardic acut, accidentele vasculare cerebrale tromboembolice și tromboembolismul pulmonar..
Structura moleculei
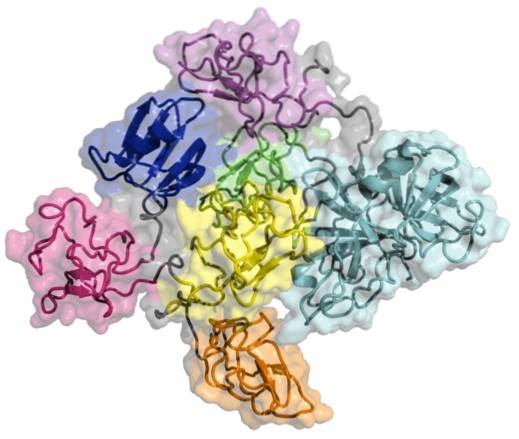
Tenecteplaza este o glicoproteină care are 527 de aminoacizi în structura sa primară și în care se disting două domenii de bază, unul numit domeniul kringle și celălalt corespunzător domeniului protează.
Domeniul kringle este o zonă a proteinei care se pliază în bucle mari care sunt stabilizate prin legături disulfidice. Acest tip de domeniu este foarte important deoarece permite interacțiunile proteină-proteină care apar cu factori de coagulare a sângelui și își primește numele de la un tort scandinav a cărui formă seamănă..
Domeniul proteazei este zona moleculei care are activitatea proteolitică care conferă enzimei însăși funcția sa de activare..
Structura moleculei este foarte asemănătoare cu cea a tPA umană naturală, cu toate acestea, tehnologia ADN-ului recombinant a permis introducerea unor modificări în ADN-ul său complementar (ADNc) care conferă proteinei codificate în ea unele avantaje terapeutice.
Modificările menționate includ înlocuirea treoninei în poziția 103 cu asparagină și asparagina 117 cu glutamină, modificări care sunt localizate în domeniul kringle; în timp ce în domeniul proteazei s-a realizat un ansamblu de tetra-alanină în domeniul pozițional 296-299.
Mecanism de acțiune
Mecanismul de acțiune al tenecteplazei este similar cu cel al tPA natural. Odată ce trombul s-a format, plasminogenul în forma sa inactivă se leagă de fibrină fără a exercita nicio acțiune proteolitică asupra acestuia..
TPA produs de celulele endoteliale se leagă de fibrină, dobândind astfel proprietatea sa de activare a plasminogenului în plasmină, o substanță care declanșează fibrinoliza.
Modificările produse în molecula tPA și încorporate în tenecteplază fac acțiunea de activare a substanței menționate asupra plasminogenului mai sensibilă la prezența fibrinei. Specificitatea fibrinei care limitează acțiunea sa la siturile trombului și reduce activarea sistemică a plasminogenului și degradarea rezultată a fibrinogenului plasmatic.
Prezentare
Dozajul sau potența substanței este exprimată în mg și în unități (U) de tenecteplază. Unitățile reprezintă un standard de referință specific pentru medicament și nu sunt comparabile cu unitățile altor agenți trombolitici. Un mg este egal cu 200 de unități (U).
O formă de afaceri este Metalyse, care vine în două prezentări, fiecare dintre ele având un flacon cu produsul sub formă de pulbere albă și o seringă preumplută cu solvent, transparent și incolor, pentru reconstituirea acestuia.
Într-una dintre ele flaconul conține 8000 de unități (40 mg) și seringa 8 ml de solvent. În celălalt flacon conține 10.000 U (50 mg) și seringa 10 ml. În ambele cazuri, odată ce soluția este reconstituită prin adăugarea conținutului seringii în flaconul corespunzător, aceasta va conține 1000 de unități (5 mg) pentru fiecare ml și va apărea limpede și incoloră, sau ușor galbenă..
Doza
Tratamentul cu tenecteplază trebuie început cât mai repede posibil, în decurs de 6 ore de la apariția simptomelor. Datorită riscurilor implicite de sângerare sau hemoragie, acesta trebuie prescris de către medici cu experiență în tratamentul trombolitic și în instituții cu mijloace de monitorizare și contracarare a acestui tip de efecte secundare..

Dozajul substanței trebuie să se bazeze pe greutatea corporală, cu o doză minimă de 6000 de unități, echivalentă cu 30 mg dizolvată într-un volum de 6 ml de soluție reconstituită, pentru a fi administrată la pacienții cu greutatea corporală sub 60 kg..
Doza maximă este de 10.000 U (50 mg / 10 ml soluție) rezervată pacienților cu greutatea corporală de 90 kg sau mai mult..
Programul de dozare pentru pacienții ale căror greutăți sunt cuprinse între 60 și sub 90 kg este după cum urmează:
- ≥ 60 a < 70 = 7000 U (35 mg/7 ml)
- ≥ 70 a < 80 = 8000 U (40 mg/8 ml)
- ≥ 80 a < 90 = 9000 U (45 mg/9 ml)
Doza necesară trebuie administrată sub formă de bolus intravenos unic și pe o perioadă de aproximativ 10 secunde. Poate fi administrat printr-un circuit intravenos conectat anterior și prin care se trece o soluție fiziologică de clorură de sodiu 0,9% (9 mg / ml).
Medicamentul este incompatibil cu soluțiile de glucoză și, deși, conform criteriilor terapeutice actuale, tratamentul adjuvant antitrombotic care ar putea include agenți antiplachetari și anticoagulanți trebuie administrat în paralel, nu trebuie adăugat niciun alt medicament la soluția injectabilă de tenecteplază..
Referințe
- Balsera, E. C., Palomino, M. Á. P., Ordoñez, J. M., Caler, C. L., Paredes, T. G. și García, G. Q. (2011). Eficacitatea și siguranța alteplazei versus tenecteplazei în fibrinoliza sindromului coronarian acut cu creștere ST. Cardiocore, 46(4), 150-154.
- Bauer C și Walzog B: Blut: ein Flüssiges Organsystem, în: Fiziologie, Ediția a 6-a; R Klinke și colab. (Eds). Stuttgart, Georg Thieme Verlag, 2010.
- Fatovich, D. M., Dobb, G. J. și Clugston, R. A. (2004). Un studiu pilot randomizat de tromboliză în stop cardiac (Procesul TICA). Resuscitare, 61(3), 309-313.
- Guyton AC, Sala JE: Hemostază și coagulare a sângelui, în: Manual de fiziologie medicală , Ediția a 13-a, AC Guyton, JE Hall (ed.). Philadelphia, Elsevier Inc., 2016.
- Haley Jr, E. C., Lyden, P. D., Johnston, K. C., Hemmen, T. M. și TNK în Stroke Investigators. (2005). Un studiu pilot de siguranță a creșterii dozei de tenecteplază în AVC ischemic acut. Accident vascular cerebral, 36(3), 607-612.
- Jelkman W: Blut, în: Physiologie des Menschen mit Pathophysiologie, Ed. 31, RF Schmidt și colab. (Eds). Heidelberg, Springer Medizin Verlag, 2010.


Nimeni nu a comentat acest articol încă.