
Caracteristicile, structura, funcțiile peroxidazei de iod
peroxidaza de iod o peroxidaza tiroidiană (TPO) este o hemoglicoproteină care aparține familiei peroxidazelor mamifere (cum ar fi mieloperoxidaza, lactoperoxidaza și altele) care participă la calea de sinteză a hormonilor tiroidieni.
Funcția sa principală este "iodarea" reziduurilor de tirozină din tiroglobulină și formarea 3-3'-5-triiodotironinei (T3) și tiroxinei (T4) printr-o reacție de "cuplare". Intramoleculară a tirozinelor iodate..
Triiodotironina și tiroxina sunt doi hormoni produși de glanda tiroidă care au funcții esențiale în dezvoltarea, diferențierea și metabolismul mamiferelor. Mecanismul său de acțiune depinde de interacțiunea receptorilor săi nucleari cu secvențele genetice specifice ale genelor sale țintă..
Existența enzimei iodură peroxidază a fost confirmată în anii 1960 de diferiți autori și s-au făcut progrese considerabile în ceea ce privește determinarea structurii acesteia, a funcțiilor sale și a caracteristicilor genei care o codifică în diferite organisme..
În mare parte din literatura de specialitate legată de această enzimă, este cunoscută sub numele de „autoantigen” microsomal și este legată de unele boli tiroidiene autoimune..
Datorită caracteristicilor sale imunogene, această enzimă este o țintă sau o moleculă țintă pentru anticorpii prezenți în serul multor pacienți cu patologii tiroidiene și defectele sale pot duce la deficiențe hormonale care pot fi importante fiziopatologic vorbind.
Indice articol
- 1 Caracteristici
- 1.1 Reglementarea expresiei
- 2 Structura
- 3 Funcții
- 3.1 Care este sinteza hormonului tiroidian?
- 4 Boli conexe
- 5 Referințe
Caracteristici
Peroxidaza de iod este codificată de o genă localizată pe cromozomul 2 la om, care măsoară peste 150 kbp și este compusă din 17 exoni și 16 introni..
Această proteină transmembranară, cu un singur segment cufundat în membrană, este strâns legată de mieloperoxidaza, cu care împărtășește mai mult de 40% similaritatea secvenței de aminoacizi..
Sinteza sa are loc în poliribozomi (un set de ribozomi care este responsabil pentru traducerea aceleiași proteine) și este apoi introdus în membrana reticulului endoplasmatic, unde suferă un proces de glicozilare.
Odată sintetizată și glicozilată, peroxidaza de iod este transportată către polul apical al tirocitelor (celule tiroidiene sau celule tiroidiene), unde este capabil să-și expună centrul catalitic lumenului folicular al tiroidei..
Reglementarea expresiei
Exprimarea genei care codifică peroxidaza tiroidiană sau peroxidaza iodată este controlată de factori de transcripție specifici tiroidei, cum ar fi TTF-1, TTF-2 și Pax-8.
Elementele genetice care permit creșterea sau îmbunătățirea expresiei acestei gene la oameni au fost descrise în regiunile care flancează capătul 5 'al acesteia, de obicei între primele 140 de perechi de baze ale acestei regiuni „flancante”..
Există, de asemenea, elemente care reprimă sau scad expresia acestei proteine, dar spre deosebire de „potențatori”, acestea au fost descrise în aval de secvența genică..
O mare parte din reglarea expresiei genetice a iodurii peroxidazei are loc într-o manieră specifică țesutului, iar aceasta depinde de acțiunea elementelor de legare a ADN-ului care acționează asupra cis, precum factorii de transcripție TTF-1 și alții.
Structura
Această proteină cu activitate enzimatică are în jur de 933 de reziduuri de aminoacizi și un capăt extracelular C-terminal de 197 de aminoacizi lung care provine din expresia altor module genetice care codifică alte glicoproteine..
Greutatea sa moleculară este de aproximativ 110 kDa și face parte din grupul proteinelor transmembranare glicozilate de tip 1, deoarece are un segment transmembranar glicozilat și o grupă hem în situl său activ..
Structura acestei proteine are cel puțin o punte disulfură în regiunea extracelulară care formează o buclă închisă caracteristică, care este expusă pe suprafața tirocitelor..
Caracteristici
Funcția fiziologică principală a peroxidazei de iod este legată de participarea sa la sinteza hormonului tiroidian, unde catalizează „iodarea” reziduurilor de tirozină de monoiodotirozină (MIT) și diiodotirozină (DIT), pe lângă cuplarea reziduurilor de iodotirozină în tiroglobulină.
Care este sinteza hormonului tiroidian?
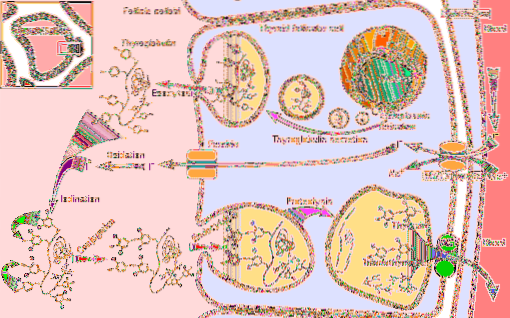
Pentru a înțelege funcția enzimei peroxidazei tiroidiene, este necesar să se ia în considerare etapele sintezei hormonale la care participă:
1-Începe cu transportul iodurii către tiroidă și continuă cu
2-Generarea unui agent oxidant precum peroxidul de hidrogen (H2O2)
3-Ulterior, se sintetizează o proteină receptoră, tiroglobulina
4-Iodura este oxidată la o stare de valență mai mare și apoi
5-Iodura se leagă de reziduurile de tirozină prezente în tiroglobulină
6-În tiroglobulină, iodotironinele (un tip de hormoni tiroidieni) se formează prin cuplarea reziduurilor de iodotirozină
7-Tiroglobulina este stocată și clivată, apoi
8-Iodul este îndepărtat din iodotirozinele libere și, în cele din urmă,
9-Tiroxina și triiodotironina sunt eliberate în sânge; Acești hormoni își exercită efectele prin interacțiunea cu receptorii lor specifici, care sunt localizați pe membrana nucleară și care sunt capabili să interacționeze cu secvențele ADN țintă, funcționând ca factori de transcripție..
Așa cum se poate deduce din cunoașterea funcțiilor celor doi hormoni la a căror sinteză participă (T3 și T4), peroxidaza de iod are implicații importante la nivel fiziologic..
Lipsa ambilor hormoni în timpul dezvoltării umane produce defecte în creștere și întârziere mintală, precum și dezechilibre metabolice în viața adultă.
Boli conexe
Iodura peroxidazei este unul dintre principalii autoantigeni tiroidieni la om și este asociată cu citotoxicitatea mediată de sistem a complementului. Funcția sa ca autoantigen este evidențiată la pacienții cu boli tiroidiene autoimune.
Boala gutei, de exemplu, se datorează unei deficiențe a conținutului de iod în timpul sintezei hormonale în tiroidă, care la rândul său a fost legată de o deficiență a iodării tiroglobulinei ca urmare a anumitor defecte ale iodurii peroxidazei..
Unele carcinoame se caracterizează prin faptul că au funcții modificate de iodură peroxidază, adică nivelurile de activitate ale acestei enzime sunt semnificativ mai mici decât la pacienții necanceri.
Cu toate acestea, studiile au confirmat că este o caracteristică foarte variabilă, care depinde nu numai de pacient, ci și de tipul de cancer și de regiunile afectate..
Referințe
- Degroot, L. J. și Niepomniszcze, H. (1977). Biosinteza hormonului tiroidian: aspecte de bază și clinice. Progrese în endocrinologie și metabolizare, 26(6), 665-718.
- Fragu, P. și Nataf, B. M. (1976). Activitatea peroxidazei tiroidiene umane în tulburările tiroidiene benigne și maligne. Societatea endocrină, Patru cinci(5), 1089-1096.
- Kimura, S. și Ikeda-saito, M. (1988). Mieloperoxidaza umană și peroxidaza tiroidiană, două enzime cu funcții fiziologice distincte și distincte, sunt membri evolutivi ai aceleiași familii genetice. Proteine: structură, funcție și bioinformatică, 3, 113-120.
- Nagasaka, A., Hidaka, H. și Ishizuki, Y. (1975). Studii privind peroxidaza de iod uman: activitatea sa în diferite tulburări tiroidiene. Clinica Chimica Acta, 62, 1-4.
- Ruf, J. și Carayon, P. (2006). Aspecte structurale și funcționale ale peroxidazei tiroidiene. Arhive de biochimie și biofizică, 445, 269-277.
- Ruf, J., Toubert, M., Czarnocka, B., Durand-gorde, M., Ferrand, M. și Carayon, P. (2015). Relația dintre structura imunologică și proprietățile biochimice ale peroxidazei tiroidiene umane. Recenzii endocrine, 125(3), 1211-1218.
- Taurog, A. (1999). Evoluția moleculară a peroxidazei tiroidiene. Biochimie, 81, 557-562.
- Zhang, J. și Lazar, M. A. (2000). Mecanismul de acțiune al hormonilor tiroidieni. Annu. Pr. Physiol., 62(1), 439-466.



Nimeni nu a comentat acest articol încă.