
Caracteristicile amilazei, clasificare, structură, funcții
Amilaza este termenul folosit pentru a identifica un grup important de enzime care este responsabil pentru hidroliza legăturilor glicozidice dintre moleculele de glucoză prezente în carbohidrați, cum ar fi amidonul și altele înrudite, care sunt ingerate în dieta multor organisme vii.
Acest tip de enzimă este produsă de bacterii, ciuperci, animale și plante, unde catalizează practic aceleași reacții și au diverse funcții, legate în principal de metabolismul energetic..
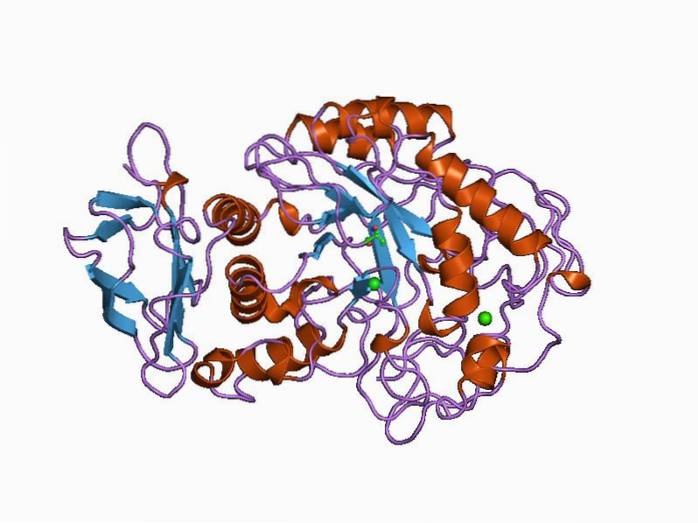
Produsele reacțiilor de hidroliză ale legăturilor glicozidice pot fi considerate caracteristice pentru fiecare tip de enzimă amilolitică, deci acesta este adesea un parametru important pentru clasificarea lor..
Importanța acestor enzime, antropocentric vorbind, nu este doar fiziologică, deoarece în prezent acest tip de enzime are o mare semnificație biotehnologică în producția industrială de alimente, hârtie, textile, zaharuri și altele..
Termenul "amilază" derivă din greaca "amylon", care înseamnă amidon și a fost inventat în 1833 de oamenii de știință Payen și Persoz, care au studiat reacțiile hidrolitice ale acestei enzime pe amidon.
Indice articol
- 1 Caracteristici
- 1.1 Caracteristicile substratului
- 2 Clasificare
- 2.1 Clasamentul actual
- 3 Funcții
- 3.1 La animale
- 3.2 La plante
- 3.3 La microorganisme
- 3.4 Utilizări industriale
- 4 Referințe
Caracteristici
Unele amilaze sunt de natură multimerică, cum ar fi β-amilaza de cartof dulce, care se comportă ca un tetramer. Cu toate acestea, greutatea moleculară aproximativă a monomerilor amilazei este în intervalul de 50 kDa..
În general, atât enzimele vegetale, cât și cele animale au o compoziție relativ „comună” de aminoacizi și au activități optime la pH între 5,5 și 8 unități (amilazele animale fiind mai active la pH mai neutru)..
Amilazele sunt enzime capabile să hidrolizeze legături glicozidice ale unei cantități mari de polizaharide, producând în general dizaharide, dar nu sunt capabile să hidrolizeze complexe precum celuloza..
Caracteristicile substratului
Motivul pentru care amilazele sunt atât de importante în natură, în special în digestia glucidelor, este legat de prezența omniprezentă a substratului lor natural (amidon) în țesuturile legumelor „superioare”, care servesc ca sursă de hrană pentru mai multe tipuri. a animalelor și a microorganismelor.
Această polizaharidă este compusă, la rândul său, din două complexe macromoleculare cunoscute sub numele de amiloză (insolubilă) și amilopectină (solubilă). Porțiunile de amiloză sunt formate din lanțuri liniare de reziduuri de glucoză legate prin legături α-1,4 și sunt degradate de α-amilaze..
Amilopectina este un compus cu greutate moleculară mare, este alcătuită din lanțuri ramificate de reziduuri de glucoză legate prin legături α-1,4, ale căror ramuri sunt susținute de legături α-1,6..
Clasificare
Enzimele amilazice sunt clasificate în funcție de locul în care sunt capabile să rupă legăturile glicozidice ca endoamilaze sau exoamilaze. Fostele se leagă în regiunile interne ale glucidelor, în timp ce acestea din urmă pot cataliza doar hidroliza reziduurilor la capetele polizaharidelor..
În plus, clasificarea tradițională este legată de stereochimia produselor lor de reacție, astfel încât aceste proteine cu activitate enzimatică sunt clasificate și ca a-amilaze, β-amilaze sau γ-amilaze..
-Α-amilazele (α-1,4-glucan 4-glucan hidrolaze) sunt endoamilaze care acționează asupra legăturilor interne ale substraturilor de conformație liniară și ale căror produse au configurație α și sunt amestecuri de oligozaharide.
-Β-amilazele (maltohidrolaze α-1,4-glucanice) sunt exoamilaze vegetale care acționează asupra legăturilor la capetele nereducătoare ale polizaharidelor precum amidonul și ale căror produse hidrolitice sunt reziduuri de β-maltoză.
-În cele din urmă, γ-amilazele sunt o a treia clasă de amilaze numite și glucoamilaze (α-1,4-glucan glucohidrolaze) care, la fel ca β-amilazele, sunt exoamilaze capabile să îndepărteze unități de glucoză unice de la capetele nereducătoare ale polizaharidelor și să le inverseze configurare.
Cea din urmă clasă de enzime poate hidroliza atât legăturile α-1,4, cât și legăturile α, 1-6, transformând substraturi precum amidonul în D-glucoză. La animale se găsesc în principal în țesutul hepatic.
Clasamentul actual
Odată cu apariția noilor tehnici de analiză biochimică atât pentru enzime, cât și pentru substraturile și produsele acestora, anumiți autori au stabilit că există cel puțin șase clase de enzime amilazice:
1-Endoamilaze care hidrolizează legăturile α-1,4 glucozidice și pot „sări” (ocolire) legături α-1,6. Exemplele acestei grupe sunt α-amilazele.
2-Exoamilazele capabile să hidrolizeze α-1,4 ale căror produse principale sunt reziduuri de maltoză și legăturile α-1,6 nu pot fi „omise”. Exemple de grup sunt β-amilazele.
3-Exoamilaze capabile să hidrolizeze legăturile α-1,4 și α-1,6 precum amiloglucozidazele (glucoamilazele) și alte exoamilazele.
4-amilaze care hidrolizează numai legăturile α-1,6 glucozidice. În acest grup se află enzimele „de ramificare” și altele cunoscute sub numele de pullulanaze..
5-amilaze precum α-glucozidazele, care hidrolizează preferențial legăturile α-1,4 ale oligozaharidelor scurte produse prin acțiunea altor enzime pe substraturi precum amiloză sau amilopectină.
6-Enzime care hidrolizează amidonul în polimeri ciclici nereducători ai reziduurilor D-glucozidice cunoscuți sub numele de ciclodextrine, cum ar fi unele amilaze bacteriene.
Caracteristici
Multe sunt funcțiile care sunt atribuite enzimelor cu activitate amilazică, nu numai din punct de vedere natural sau fiziologic, ci și din punct de vedere comercial și industrial, direct legate de om.
La animale
Amilazele la animale sunt prezente în esență în salivă, ficat și pancreas, unde mediază degradarea diferitelor polizaharide consumate în dietă (de origine animală (glicogeni) sau vegetale (amidon)).
Α-amilaza prezentă în salivă este utilizată ca indicator al stării fiziologice a glandelor salivare, deoarece reprezintă mai mult de 40% din producția de proteine a acestor glande.
În compartimentul oral, această enzimă este responsabilă de „pre-digestia” amidonului, producând reziduuri de maltoză, maltotrioză și dextrină..
În plante
La plante, amidonul este o polizaharidă de rezervă și hidroliza sa, mediată de enzimele amilazei, are multe funcții importante. Printre acestea se pot evidenția următoarele:
- Germinarea semințelor de cereale prin digestia stratului de aleuronă.
- Degradarea substanțelor de rezervă pentru achiziționarea de energie sub formă de ATP.
În microorganisme
Multe microorganisme folosesc amilaze pentru a obține carbon și energie din diverse surse de polizaharide. În industrie, aceste microorganisme sunt exploatate pentru producția pe scară largă a acestor enzime, care servesc la satisfacerea diferitelor cerințe comerciale ale omului.
Utilizări industriale
În industrie, amilazele sunt utilizate în diverse scopuri, inclusiv pentru fabricarea maltozei, siropuri bogate în fructoză, amestecuri de oligozaharide, dextrine etc..
Acestea sunt, de asemenea, utilizate pentru fermentarea alcoolică directă a amidonului în etanol în industria berii și pentru utilizarea apei reziduale produse în timpul procesării alimentelor pe bază de plante ca sursă alimentară pentru creșterea microorganismelor, de exemplu.
Referințe
- Aiyer, P. V. (2005). Amilazele și aplicațiile lor. Revista Africană de Biotehnologie, 4(13), 1525-1529.
- Azcón-Bieto, J. și Talón, M. (2008). Bazele fiziologiei plantelor (Ed. A 2-a). Madrid: McGraw-Hill Interamericana din Spania.
- Del Vigna, P., Trinidade, A., Naval, M., Soares, A. și Reis, L. (2008). Compoziția și funcțiile salivei: o revizuire cuprinzătoare. Jurnalul de practică dentară contemporană, 9(3), 72-80.
- Naidu, M. A. și Saranraj, P. (2013). Amilaza bacteriană: o recenzie. Jurnalul Internațional de Arhive Farmaceutice și Biologice, 4(2), 274-287.
- Salt, W. și Schenker, S. (1976). Amilaza - Semnificația sa clinică: o revizuire a literaturii. Medicament, 55(4), 269-289.
- Saranraj, P. și Stella, D. (2013). Fung amilaza - O recenzie. Jurnalul internațional de cercetare microbiologică, 4(2), 203-211.
- Solomon, E., Berg, L. și Martin, D. (1999). Biologie (Ed. A 5-a). Philadelphia, Pennsylvania: Editura Saunders College.
- Thoma, J. A., Spradlin, J. E. și Dygert, S. (1925). Amilaze vegetale și animale. Ann. Chem., 1, 115-189.



Nimeni nu a comentat acest articol încă.