
Caracteristici, structură, utilizări ale acidului hipobrom

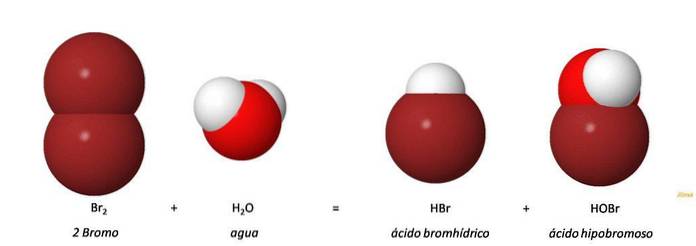
acid hipobrom (HOBr, HBrO) este un acid anorganic produs de oxidarea anionului bromură (Br-). Adăugarea de brom în apă dă acid bromhidric (HBr) și acid hipobrom (HOBr) printr-o reacție de disproporționare. Br2 + H2O = HOBr + HBr
Acidul hipobromos este un acid foarte slab, oarecum instabil, existent ca soluție diluată la temperatura camerei. Este produs în organisme vertebrate cu sânge cald (inclusiv oameni), prin acțiunea enzimei eozinofil peroxidază.
Descoperirea că acidul hipobromos poate regla activitatea colagenului IV a atras o mare atenție..
Indice articol
- 1 Structură
- 1.1 2D
- 1.2 3D
- 2 Proprietăți fizice și chimice
- 3 utilizări
- 4 Interacțiuni biomoleculare
- 5 Referințe
Structura
2D
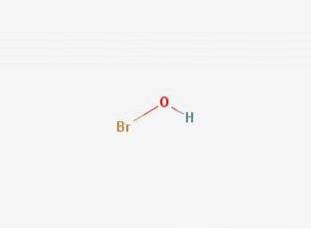
3D

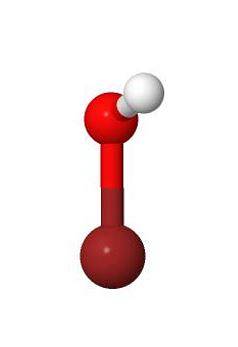
Proprietati fizice si chimice
- Aspect solid galben: solid galben.
- Aspect: solide galbene.
- Greutate moleculară: 96,911 g / mol.
- Punct de fierbere: 20-25 ° C.
- Densitate: 2.470 g / cm3.
- Aciditate (pKa): 8,65.
- Proprietățile chimice și fizice ale acidului hipobromos sunt similare cu cele ale altor hipoalite..
- Vine ca o soluție diluată la temperatura camerei.
- Solidele hipobromite sunt de culoare galbenă și au un miros aromat deosebit.
- Este un puternic bactericid și dezinfectant pentru apă.
- Are un pKa de 8,65 și se disociază parțial în apă la pH 7.
Aplicații
- Acidul hipobromos (HOBr) este utilizat ca agent de albire, oxidant, deodorant și dezinfectant, datorită capacității sale de a distruge celulele multor agenți patogeni..
- Este folosit de industria textilă ca agent de albire și uscare.
- De asemenea, utilizat în căzi cu hidromasaj și spa-uri ca agent germicid.
Interacțiuni biomoleculare
Bromul este omniprezent la animale ca bromură ionică (Br-), dar până de curând funcția sa esențială era necunoscută..
Cercetări recente au arătat că bromul este esențial pentru arhitectura membranei bazale și dezvoltarea țesuturilor.
Enzima peroxidaină folosește HOBr pentru a lega încrucișat sulfilimina, care este legată încrucișat în schelele de colagen IV ale membranei bazale..
Acidul hipobromos este produs în organismele vertebrate cu sânge cald prin acțiunea enzimei eozinofil peroxidază (EPO).
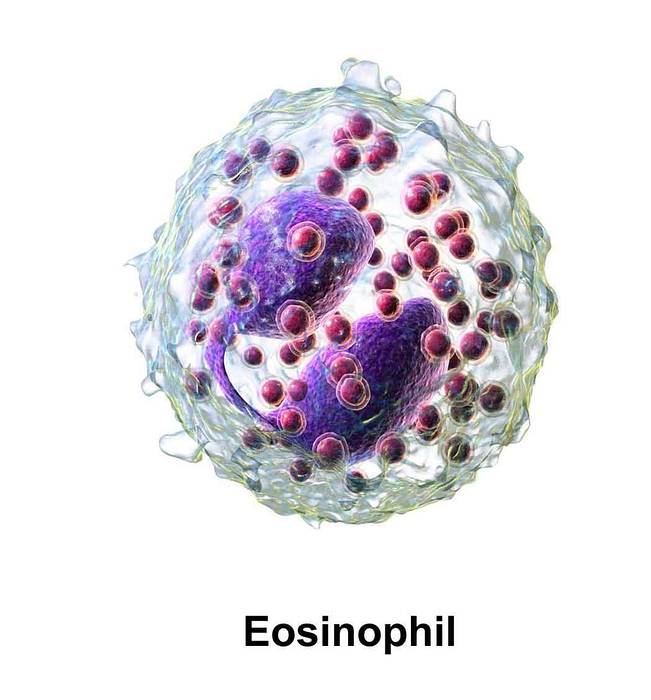
EPO generează HOBr din H2O2 și Br- în prezența unei concentrații plasmatice de Cl-.
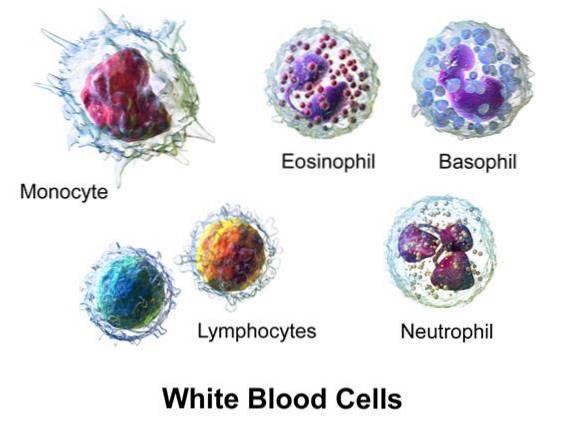
Mieloperoxidaza (MPO), din monocite și neutrofile, generează acid hipocloros (HOCl) din H2O2 și Cl-.
EPO și MPO joacă un rol important în mecanismele de apărare a gazdei împotriva agenților patogeni, folosind HOBr și respectiv HOCl.
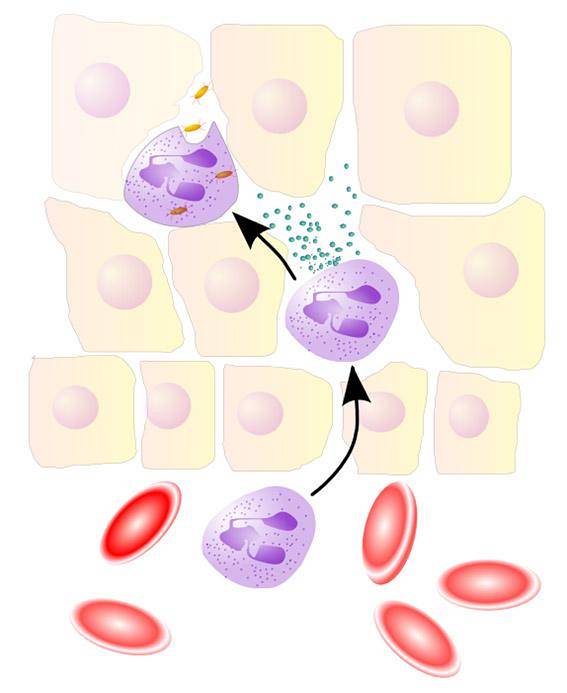
Sistemul MPO / H2O2 / Cl- în prezența Br- generează, de asemenea, HOBr prin reacția HOCl format cu Br-. Mai mult decât un oxidant puternic, HOBr este un electrofil puternic.
Concentrația plasmatică de Br- este de peste 1000 de ori mai mică decât cea a anionului clorură (Cl-). În consecință, producția endogenă de HOBr este, de asemenea, mai mică comparativ cu HOCl.
Cu toate acestea, HOBr este semnificativ mai reactiv decât HOCl atunci când oxidabilitatea compușilor studiați nu este relevantă, astfel încât reactivitatea HOBr ar putea fi mai mult asociată cu puterea sa electrofilă decât cu puterea sa de oxidare (Ximenes, Morgon & de Souza, 2015).
Deși potențialul său de redox este mai mic decât cel al HOCl, HOBr reacționează cu aminoacizii mai repede decât HOCl.
Halogenarea inelului de tirozină de către HOBr este de 5000 de ori mai rapidă decât cea a HOCl.
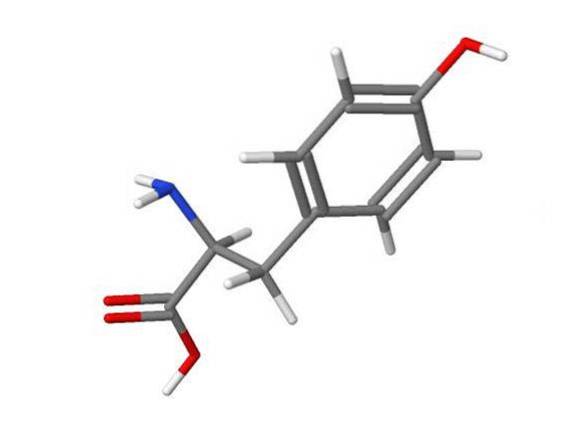
HOBr reacționează, de asemenea, cu nucleobazele nucleobazelor și ADN-ul.
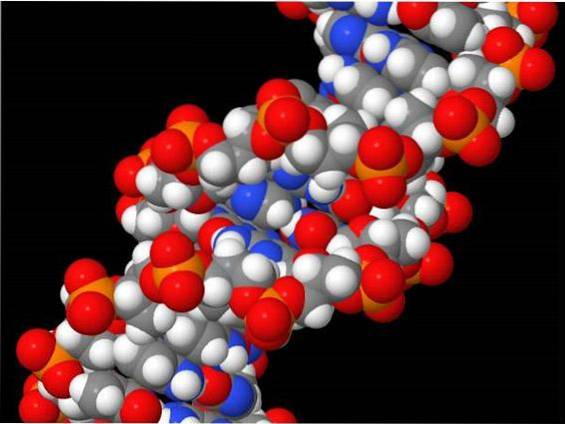
2'-deoxicitidina, adenina și guanina, generează 5-bromo-2'-deoxicitidină, 8-bromoadenină și 8-bromoguanină în sistemele EPO / H2O2 / Br- și MPO / H2O2 / Cl- / Br- (Suzuki, Kitabatake și Koide , 2016).
McCall și colab. (2014) au arătat că Br este un cofactor necesar pentru formarea de legături încrucișate cu sulfilimină catalizate de enzima peroxidasină, o modificare post-translațională esențială pentru arhitectura colagenului IV al membranelor bazale și dezvoltarea țesuturilor..
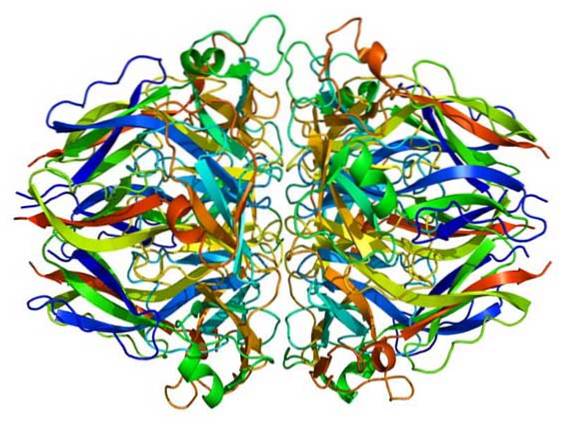
Membranele subsolului sunt matrici extracelulare specializate care sunt mediatori cheie pentru transducția semnalului și suportul mecanic al celulelor epiteliale..
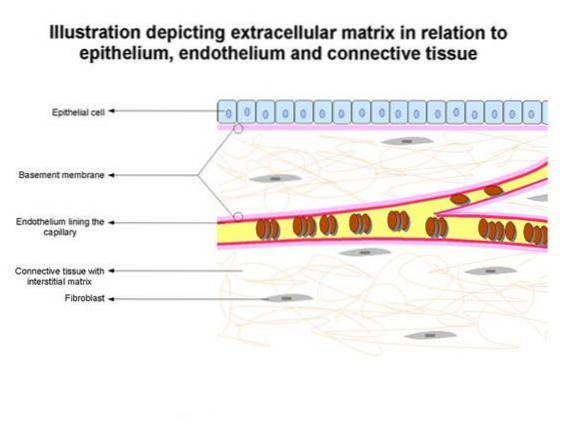
Membranele subsolului definesc arhitectura țesutului epitelial și facilitează repararea țesutului după vătămare, printre alte funcții..
Înglobată în membrana bazală este o schelă de colagen IV reticulată cu sulfilimină, care oferă funcționalitatea matricei în țesuturile multicelulare ale tuturor animalelor..
Schelele de colagen IV oferă rezistență mecanică, servesc drept ligand pentru integrine și alți receptori ai suprafeței celulare și interacționează cu factorii de creștere pentru a stabili gradienți de semnalizare..
Sulfilimina (sulfimida) este un compus chimic care conține o dublă legătură sulf-azot. Legăturile de sulfilimină stabilizează firele de colagen IV găsite în matricea extracelulară.
Aceste legături leagă covalent resturile de metionină 93 (Met93) și hidroxilizină 211 (Hyl211) ale catenelor polipeptidice adiacente pentru a forma un trimer de colagen mai mare..
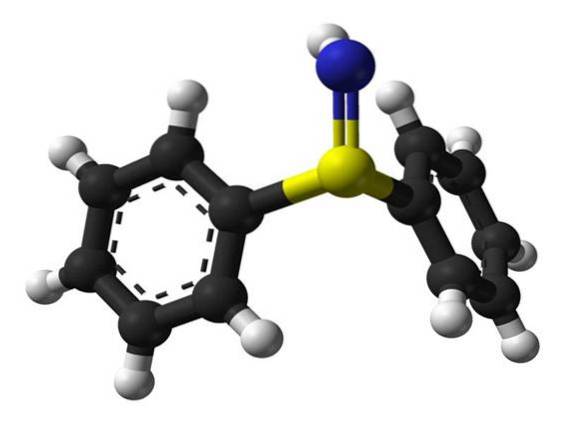
Peroxidaina formează acid hipobromos (HOBr) și acid hipocloros (HOCl) din bromură și respectiv clorură, care pot media formarea legăturilor încrucișate cu sulfilimină..
Bromura, convertită în acid hipobromos, formează un intermediar al ionului bromosulfoniu (S-Br) care participă la formarea legăturilor încrucișate.
McCall și colab. (2014) au demonstrat că deficiența alimentară de Br este letală în mușca Drosophila, în timp ce înlocuirea Br restabilește viabilitatea.
De asemenea, au stabilit că bromul este un oligoelement esențial pentru toate animalele datorită rolului său în formarea legăturilor sulfiliminei și a colagenului IV, care este de o importanță vitală pentru formarea membranelor bazale și dezvoltarea țesuturilor..
Referințe
- ChemIDplus, (2017). Structura 3D a 13517-11-8 - Acid hipobrom [imagine] Adus de la nih.gov.
- ChemIDplus, (2017). Structura 3D a 60-18-4 - tirozină [USAN: INN] [imagine] Adus de la nih.gov.
- ChemIDplus, (2017). Structura 3D a 7726-95-6 - Brom [imagine] Adus de la nih.gov.
- ChemIDplus, (2017). Structura 3D a 7732-18-5 - Apă [imagine] Recuperată de la nih.gov.
- Emw, (2009). Proteina COL4A1 PDB 1li1 [imagine] Recuperat de pe wikipedia.org.
- Mills, B. (2009). Difenilsulfimidă-din-xtal-2002-3D-bile [imagine] Recuperat de pe wikipedia.org.
- PubChem, (2016). Acid hipobrom [imagine] Adus de la nih.gov.
- Steane, R. (2014). Molecula ADN - rotativă în 3 dimensiuni [imagine] Recuperat de pe biotopics.co.uk
- Thormann, U. (2005). NeutrophilerAktion [imagine] Recuperat de pe wikipedia.org.


Nimeni nu a comentat acest articol încă.