
Structura, proprietățile, utilizările și exemplele aldehidelor

aldehide sunt compuși organici care au formula generală RCHO. R reprezintă un lanț alifatic sau aromatic; C la carbon; O la oxigen și H la hidrogen. Acestea se caracterizează prin faptul că au o grupă carbonil precum cetone și acizi carboxilici, motiv pentru care aldehidele sunt numite și compuși carbonilici.
Gruparea carbonil conferă aldehidei multe dintre proprietățile sale. Sunt compuși care se oxidează ușor și sunt foarte reactivi la adaosurile nucleofile. Legătura dublă a grupării carbonil (C = O) are doi atomi care au diferențe în lăcomia lor pentru electroni (electronegativitate).
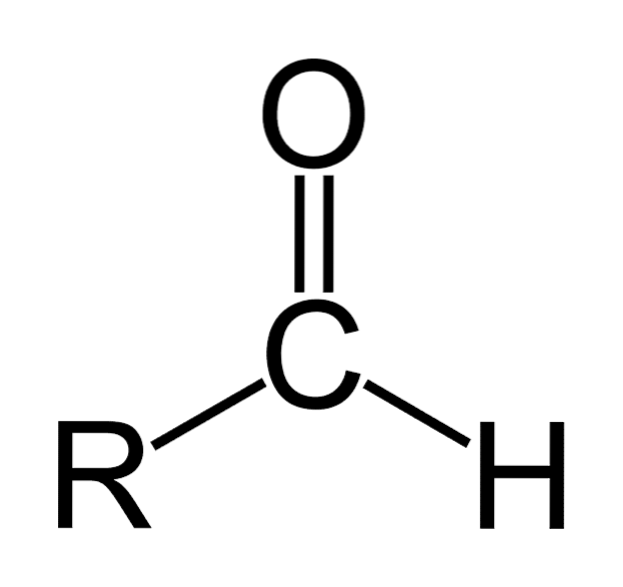
Oxigenul atrage electronii cu o forță mai mare decât carbonul, astfel încât norul de electroni se deplasează spre el, făcând legătura dublă dintre carbon și oxigen polar în natură, cu un moment dipol semnificativ. Acest lucru face ca aldehidele să fie compuși polari..
Polaritatea aldehidelor le va influența proprietățile fizice. Punctul de fierbere și solubilitatea aldehidelor în apă sunt mai mari decât compușii chimici nepolari cu greutăți moleculare similare, așa este cazul hidrocarburilor..
Aldehidele cu mai puțin de cinci atomi de carbon sunt solubile în apă, deoarece legăturile de hidrogen se formează între oxigenul grupării carbonil și molecula apei. Cu toate acestea, creșterea numărului de carboni din lanțul de hidrocarburi produce o creștere a porțiunii nepolare a aldehidei, făcându-l mai puțin solubil în apă..
Dar cum sunt și de unde vin? Deși natura sa depinde în esență de gruparea carbonil, restul structurii moleculare contribuie, de asemenea, mult la întreg. Astfel, pot fi de orice dimensiune, mici sau mari, sau chiar o macromoleculă poate avea regiuni în care predomină caracterul aldehidelor..
Astfel, la fel ca în cazul tuturor compușilor chimici, există aldehide „plăcute” și alți amari. Ele pot fi găsite în surse naturale sau sintetizate pe scară largă. Exemple de aldehide sunt vanilina, foarte prezentă în înghețatele (imaginea de sus) și acetaldehida, care adaugă aromă băuturilor alcoolice..
Indice articol
- 1 Structura chimică
- 2 Proprietăți fizice și chimice
- 2.1 Puncte de topire
- 2.2 Puncte de fierbere
- 2.3 Solubilitatea în apă exprimată în g / 100 g H2O
- 3 Reactivitate
- 3.1 Reacția de oxidare
- 3.2 Reducerea la alcooli
- 3.3 Reducerea la hidrocarburi
- 3.4 Adaos nucleofil
- 4 Nomenclatură
- 5 utilizări
- 5.1 Formaldehidă
- 5.2 Bakelită
- 5.3 Placaj
- 5.4 Poliuretan
- 5.5 Butiraldehidă
- 5.6 Acetaldehidă
- 5.7 Sinteza
- 6 Exemple de aldehide
- 6.1 Glutaraldehidă
- 6.2 Benzaldehidă
- 6.3 Gliceraldehidă
- 6.4 Gliceraldehidă-3-fosfat
- 6.5 11-cis-retinian
- 6.6 Fosfat piridoxal (vitamina B6)
- 6.7 Salicilaldehidă
- 7 Referințe
Structura chimică

Aldehidele constau dintr-un carbonil (C = O) de care este atașat direct un atom de hidrogen. Acest lucru îl diferențiază de alți compuși organici, cum ar fi cetonele (RDouăC = O) și acizi carboxilici (RCOOH).
Imaginea superioară arată structura moleculară din jurul -CHO, o grupare formil. Grupul formil este plat deoarece carbonul și oxigenul au hibridizare spDouă. Această planaritate o face susceptibilă la atacul speciilor nucleofile și, prin urmare, este ușor oxidată..
La ce se referă această oxidare? La formarea unei legături cu orice alt atom mai electronegativ decât carbonul; iar în cazul aldehidelor este un oxigen. Astfel, aldehida este oxidată la un acid carboxilic, -COOH. Ce se întâmplă dacă aldehida a fost redusă? În locul său s-ar forma un alcool primar, ROH.
Aldehidele sunt produse numai din alcooli primari: cei în care grupul OH se află la capătul unui lanț. În mod similar, gruparea formil pentru totdeauna este la capătul unui lanț sau iese din acesta sau din inel ca substituent (dacă există alte grupuri mai importante, cum ar fi -COOH).
Proprietati fizice si chimice
Deoarece sunt compuși polari, punctele lor de topire sunt mai mari decât cele ale compușilor nepolari. Moleculele de aldehidă nu sunt capabile de legături intermoleculare prin legături de hidrogen, deoarece au doar atomi de carbon atașați la atomii de hidrogen..
Datorită celor de mai sus, aldehidele au puncte de fierbere mai mici decât alcoolii și acizii carboxilici.
Puncte de topire
Formaldehidă -92; Acetaldehidă -121; Propionaldehidă -81; n-butiraldehidă -99; n-Valeraldehidă -91; Caproaldehidă -; Heptaldehidă - 42; Fenilacetaldehidă -; Benzaldehidă -26.
Puncte de fierbere
Formaldehidă -21; Acetaldehidă 20; Propionaldehidă 49; n-butiraldehidă 76; n-Valeraldehidă 103; Caproaldehidă 131; Heptaldehidă 155; Fenilacetaldehidă 194; Benzaldehidă 178.
Solubilitatea în apă exprimată în g / 100 g de HDouăSAU
Formaldehidă, foarte solubilă; Acetaldehidă, infinită; Propionaldehidă, 16; n-butiraldehidă, 7; n-Valeraldehidă, ușor solubilă; caproaldehidă, ușor solubilă; Fenilacetaldehidă ușor solubilă; Benzaldehidă, 0,3.
Punctele de fierbere ale aldehidelor tind să crească direct cu greutatea moleculară. Dimpotrivă, există o tendință de scădere a solubilității aldehidelor în apă pe măsură ce crește greutatea lor moleculară. Acest lucru se reflectă în constantele fizice ale aldehidelor menționate anterior..
Reactivitate
Reacție de oxidare
Aldehidele pot fi oxidate la acidul carboxilic corespunzător în prezența oricăruia dintre acești compuși: Ag (NH3)Două, KMnO4 BineDouăCrDouăSAU7.
Reducerea la alcooli
Pot fi hidrogenate cu ajutorul catalizatorilor de nichel, platină sau paladiu. Astfel, C = O devine C-OH.
Reducerea la hidrocarburi
În prezența Zn (Hg), HCI concentrat sau în NHDouăNHDouă aldehidele pierd gruparea carbonil și devin hidrocarburi.
Adaos nucleofil
Există mai mulți compuși care se adaugă la gruparea carbonil, printre care se numără: reactivi Grignard, cianură, derivați de amoniac și alcooli.
Nomenclatură
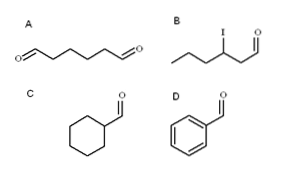
Patru aldehide sunt ilustrate în imaginea de mai sus. Cum sunt numite?
Deoarece sunt alcooli primari oxidați, numele alcoolului se schimbă din -ol în -al. Astfel, metanolul (CH3OH) dacă este oxidat la CH3CHO se numește metanal (formaldehidă); CH3CHDouăCHO etanal (acetaldehidă); CH3CHDouăCHDouăCHO propanal și CH3CHDouăCHDouăCHDouăCHO butanal.
Toate aldehidele nou numite au grupul -CHO la capătul lanțului. Când se găsește la ambele capete, ca și la A, terminația -al este precedată de prefixul di-. Deoarece A are șase atomi de carbon (numărându-i pe cei din ambele grupări formil), derivă din 1-hexanol și, prin urmare, numele său este: hexanformează.
Când există un substituent, cum ar fi un radical alchil, o legătură dublă sau triplă sau un halogen, carbonii din lanțul principal sunt enumerați dând -CHO numărul 1. Astfel, aldehida B se numește: 3-iodohexanal.
Cu toate acestea, în aldehidele C și D grupul -CHO nu are prioritate pentru a identifica astfel de compuși de alții. C este un cicloalcan, în timp ce D un benzen, ambii cu unul dintre Hs lor substituiți cu o grupare formil.
În ele, deoarece structura principală este ciclică, gruparea formil este denumită carbaldehidă. Astfel, C este ciclohexanecarbaldehidă, iar D este benzenecarbaldehidă (mai bine cunoscută sub numele de benzaldehidă).
Aplicații
Aldehidele există în natură, capabile să confere arome plăcute, așa este cazul cinamaldehidei, responsabilă de aroma caracteristică a scorțișoarei. De aceea sunt adesea folosite ca arome artificiale în multe produse precum dulciurile sau alimentele..
Formaldehida
Formaldehida este aldehida cea mai produsă industrial. Formaldehida obținută prin oxidarea metanolului este utilizată într-o soluție de 37% din gaz în apă, sub denumirea de formalină. Aceasta este utilizată la tăbăcirea pieilor și la conservarea și îmbălsămarea cadavrelor..
La fel, formaldehida este utilizată ca germicid, fungicid și insecticid pentru plante și legume. Cu toate acestea, cea mai mare utilitate a acestuia este contribuția la producția de material polimeric. Plasticul numit bakelit este sintetizat prin reacția dintre formaldehidă și fenol.
Bachelită
Bakelitul este un polimer foarte dur cu o structură tridimensională utilizată în multe ustensile de uz casnic, cum ar fi mânerele pentru oale, tigăi, aparate de cafea, cuțite etc..
Polimerii de tip bakelit sunt fabricați din formaldehidă în combinație cu compușii uree și melamină. Acești polimeri sunt utilizați nu numai ca materiale plastice, ci și ca adezivi adezivi și material de acoperire..
Placaj
Placajul este denumirea comercială a unui material format din foi subțiri de lemn, unite de polimeri produși din formaldehidă. Marcile Formica și Melmac sunt fabricate cu participarea acestuia din urmă. Formica este un material plastic utilizat la acoperirea mobilierului.
Plasticul Melmac este folosit pentru a face farfurii, pahare, cupe etc. Formaldehida este materia primă pentru sinteza compusului metilen-difenil-diizocianat (MDI), un precursor al poliuretanului.
Poliuretan
Poliuretanul este folosit ca izolator în frigidere și congelatoare, căptușeală pentru mobilier, saltele, acoperiri, adezivi, tălpi etc..
Butiraldehidă
Butiraldehida este principalul precursor pentru sinteza 2-etilhexanolului, care este folosit ca plastifiant. Are o aromă plăcută de mere care permite utilizarea sa în alimente ca aromă.
Este, de asemenea, utilizat pentru producerea de acceleratoare de cauciuc. Intervine ca reactiv intermediar la fabricarea solvenților.
Acetaldehidă
Acetaldehida a fost utilizată la producerea acidului acetic. Dar acest rol al acetaldehidei a scăzut din importanță, deoarece a fost deplasat de procesul de carbonilare al metanolului..
Sinteză
Alte aldehide sunt precursori ai oxoalcoolilor, care sunt utilizați în producția de detergenți. Așa-numiții oxoalcooli sunt preparați prin adăugarea de monoxid de carbon și hidrogen la o olefină pentru a obține o aldehidă. Și în cele din urmă aldehida este hidrogenată pentru a obține alcoolul.
Unele aldehide sunt utilizate la fabricarea parfumurilor, cum este cazul Chanel nr. 5. Multe aldehide de origine naturală au mirosuri plăcute, de exemplu: heptanalul are un miros de iarbă verde; octanal un miros portocaliu; nonanal un miros de trandafiri și citral un miros de tei.
Exemple de aldehide
Glutaraldehidă
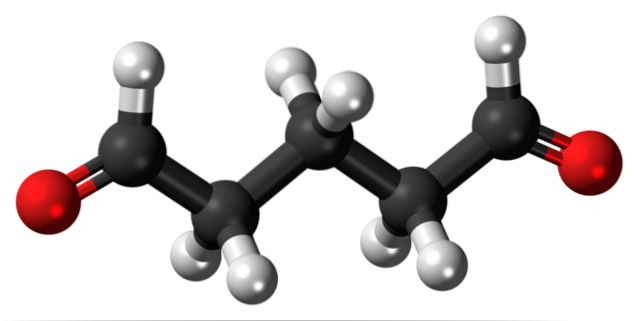
Glutaraldehida are două grupări formil în structura sa la ambele capete.
Comercializat sub denumirea de Cidex sau Glutaral, este folosit ca dezinfectant pentru sterilizarea instrumentelor chirurgicale. Se folosește pentru tratarea negilor de pe picioare, aplicându-l ca lichid. De asemenea, este utilizat ca agent de fixare a țesuturilor în laboratoarele de histologie și patologie..
Benzaldehidă
Este cea mai simplă aldehidă aromatică care este formată dintr-un inel benzenic în care este legată o grupare formil.
Se găsește în uleiul de migdale, de unde și mirosul său caracteristic care îi permite să fie folosit ca aromă alimentară. În plus, este utilizat în sinteza compușilor organici legați de fabricarea medicamentelor și în fabricarea materialelor plastice..
Gliceraldehidă
Este o aldotrioză, un zahăr format din trei atomi de carbon. Are doi izomeri numiți enantiomeri D și L. Gliceraldehida este prima monozaharidă obținută în fotosinteză în timpul fazei întunecate (ciclul Calvin)..
Gliceraldehidă-3-fosfat
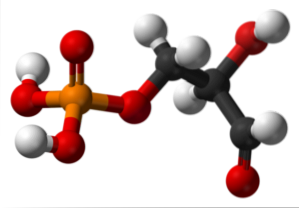
Imaginea superioară ilustrează structura gliceraldehidei-3-fosfatului. Sferele roșii de lângă galben corespund grupului fosfat, în timp ce cele negre sunt scheletul de carbon. Sfera roșie legată de cea albă este grupul OH, dar atunci când este legată de sfera neagră și cea din urmă de cea albă, atunci este grupul CHO.
Gliceraldehida-3-fosfatul este implicat în glicoliză, un proces metabolic în care glucoza este degradată în acid piruvic cu producerea de ATP, un rezervor de energie al ființelor vii. Pe lângă producția de NADH, un agent biologic de reducere.
În glicoliză, gliceraldehida-3-fosfatul și dihidroacetona fosfatul provin din clivajul D-fructozei-1-6-bisfosfatului
Gliceraldehida-3-fosfatul este implicat în procesul metabolic cunoscut sub numele de ciclul pentozei. În el se generează NADPH, un important reductor biologic..
11-cis-retinian
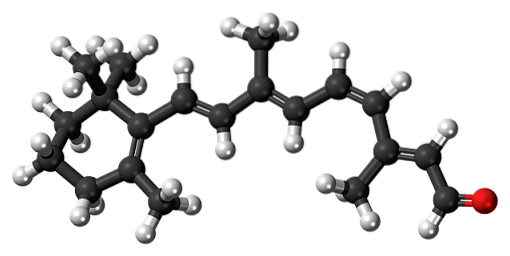
Β-carotenul este un pigment natural prezent în diferite legume, în special morcovi. Acesta suferă o descompunere oxidativă a ficatului, transformându-se astfel în alcool retinolic sau vitamina A. Oxidarea vitaminei A și izomerizarea ulterioară a uneia dintre legăturile sale duble, formează aldehida 11-cis-retinală.
Fosfat piridoxal (vitamina B6)
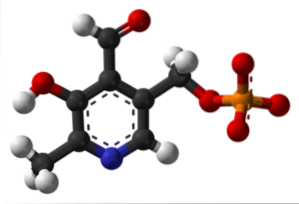
Este un grup protetic legat de mai multe enzime, care este forma activă a vitaminei B6 și participă la procesul de sinteză a neurotransmițătorului inhibitor GABA.
Unde este grupul formil în structura ta? Rețineți că acest lucru diferă de restul grupurilor legate de inelul aromatic.
Salicilaldehidă
Este o materie primă pentru sinteza acidului acetilsalicilic, un medicament analgezic și antipiretic cunoscut sub numele de Aspirină..
Referințe
- Robert C. Neuman, Jr. Capitolul 13, Compuși carbonilici: cetone, aldehide, acizi carboxilici. [PDF]. Luat de la: chem.ucr.edu
- Germán Fernández. (14 septembrie 2009). Nomenclatura aldehidelor. Luat de pe: quimicaorganica.net
- T.W. Graham Solomons, Craigh B. Fryhle. Chimie organica. (Ediția a zecea, p. 729-731) Wiley Plus.
- Jerry March și William H. Brown. (31 decembrie 2015). Aldehidă. Preluat de pe: britannica.com
- Wikipedia. (2018). Aldehidele. Luat de pe: https://en.wikipedia.org/wiki/Aldehyde
- Morrison, R. T. și Boyd, R. N. (1990). A cincea ediție de chimie organică. Editorial Addison-Wesley Iberoamericana.
- Carey, F. A. (2006). Ediția a șasea de chimie organică. Editura Mc Graw Hill.
- Mathews, Ch. K., Van Holde, K. E. și Athern, K. G. (2002). Biochimie. A treia editie. Editura Pearson Adisson Wesley.



Nimeni nu a comentat acest articol încă.