
Compresibilitatea solidelor, lichidelor, gazelor, exemple
compresibilitate a unei substanțe sau a unui material este schimbarea de volum pe care o experimentează atunci când este supusă unei schimbări de presiune. În general, volumul scade atunci când se aplică presiune asupra unui sistem sau obiect. Cu toate acestea, uneori se întâmplă opusul: o modificare a presiunii poate produce o explozie în care sistemul crește în volum sau când are loc o schimbare de fază..
În unele reacții chimice acest lucru se poate întâmpla și în gaze, de asemenea, deoarece odată cu creșterea frecvenței coliziunilor, au loc forțele respingătoare..

Când vă imaginați cât de ușor sau dificil poate fi să comprimați un obiect, luați în considerare cele trei stări în care se află în mod normal materia: solid, lichid și gazos. În fiecare dintre ele moleculele păstrează anumite distanțe unele de altele. Cu cât legăturile care unesc moleculele substanței care alcătuiesc obiectul sunt mai puternice și cu cât acestea sunt mai apropiate, cu atât va fi mai dificil să provoace o deformare.
Un solid are moleculele foarte apropiate și, atunci când încearcă să le apropie, apar forțe respingătoare care îngreunează sarcina. Prin urmare, se spune că solidele nu sunt foarte compresibile. În moleculele lichidelor există mai mult spațiu, astfel încât compresibilitatea lor este mai mare, dar chiar și așa schimbarea volumului necesită de obicei forțe mari.
Deci solidele și lichidele sunt greu de comprimat. Ar fi nevoie de o variație foarte mare a presiunii pentru a realiza o schimbare de volum apreciabilă în așa-numitele condiții normale de presiune și temperatură. Pe de altă parte, gazele, având în vedere că moleculele lor sunt la distanță mare, sunt ușor comprimate și decomprimate.
Indice articol
- 1 Compresibilitatea solidelor
- 1.1 -Comprimibilitatea unui material
- 2 Exerciții-exemple rezolvate
- 2.1 - Exercițiu rezolvat 1
- 2.2 - Exercițiu rezolvat 2
- 2.3 - Exercițiu rezolvat 3
- 3 Compresibilitatea în gaze
- 3.1 - Exercițiu rezolvat 5
- 4 Referințe
Compresibilitate solidă
De exemplu, atunci când un obiect este scufundat într-un fluid, acesta exercită presiune asupra obiectului în toate direcțiile. În acest fel putem crede că volumul obiectului va scădea, deși în majoritatea cazurilor acest lucru nu va fi apreciat..
Situația poate fi văzută în următoarea figură:
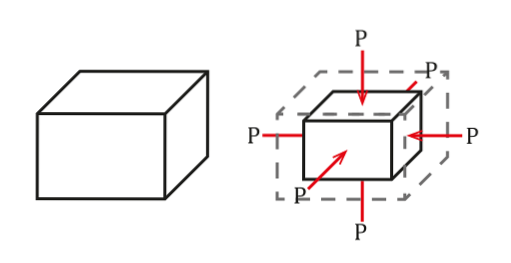
Presiunea este definită ca forță pe unitate de suprafață, ceea ce va determina o modificare a volumului ΔV proporțional cu volumul inițial al obiectului Vsau. Această modificare a volumului va depinde de calitățile sale..
Legea lui Hooke afirmă că deformarea experimentată de un obiect este proporțională cu stresul aplicat acestuia:
Stresul ∝ Tulpina
Deformarea volumetrică experimentată de un corp este cuantificată de B constanta de proporționalitate necesară, care se numește modulul volumetric al materialului:
B = -Stress / Strain
B = -ΔP / (ΔV / Vsau)
Ca ΔV / Vsau este o cantitate adimensională, deoarece este coeficientul dintre două volume, modulul volumetric are aceleași unități de presiune, care în sistemul internațional sunt Pascali (Pa).
Semnul negativ indică reducerea așteptată a volumului, atunci când obiectul este suficient de comprimat, adică presiunea crește.
-Comprimabilitatea unui material
Valoarea inversă sau reciprocă a modulului volumetric este cunoscută sub numele de compresibilitate și se notează cu litera k. Prin urmare:

Aici k este negativul modificării fracționate a volumului pe creștere a presiunii. Unitățile sale din sistemul internațional sunt inversele Pa, adică mDouă / N.
Ecuația pentru B sau pentru k, dacă preferați, este aplicabilă atât solidelor, cât și lichidelor. Conceptul de modul volumetric este rar aplicat gazelor. Un model simplu pentru a cuantifica scăderea volumului pe care îl poate experimenta un gaz real este explicat mai jos..
Viteza sunetului și modulul de compresibilitate
O aplicație interesantă este viteza sunetului într-un mediu, care depinde de modulul său de compresibilitate:

Exerciții-exemple rezolvate
-Exercițiu rezolvat 1
O sferă solidă de alamă al cărei volum este de 0,8 m3 este aruncat în ocean la o adâncime în care presiunea hidrostatică este cu 20 M Pa mai mare decât la suprafață. Cum se va schimba volumul sferei? Se știe că modulul de compresibilitate al alamei este B = 35.000 MPa,
Soluţie
1 M Pa = 1 Mega pascal = 1. 10 6 Pa
Variația presiunii față de suprafață este DP = 20 x 10 6 Pa. Aplicând ecuația dată pentru B, avem:
B = -ΔP / (ΔV / Vsau)
Prin urmare:

ΔV = -5.71.10 -4 x 0,8 m3 = -4,57 x 10-4 m3
Diferența de volum poate avea un semn negativ atunci când volumul final este mai mic decât volumul inițial, prin urmare acest rezultat este de acord cu toate ipotezele pe care le-am făcut până acum.
Modulul foarte ridicat de compresibilitate indică faptul că este necesară o schimbare mare a presiunii pentru ca obiectul să experimenteze o scădere apreciabilă a volumului..
-Exercițiu rezolvat 2
Așezând urechea pe șinele de cale ferată, puteți afla când unul dintre aceste vehicule se apropie în depărtare. Cât durează sunetul când călătoriți pe o șină de oțel dacă trenul este la 1 km distanță?
Date
Densitatea oțelului = 7,8 x 10 3 kg / m3
Modul de compresibilitate a oțelului = 2,0 x 10 unsprezece Pa.
Soluţie

Modulul de compresibilitate B calculat mai sus se aplică și lichidelor, deși este necesară o mare efort pentru a produce o scădere apreciabilă a volumului. Dar fluidele se pot extinde sau contracta pe măsură ce se încălzesc sau se răcesc și, în mod egal, dacă sunt depresurizate sau sub presiune..
Pentru apă în condiții standard de presiune și temperatură (0 ° C și o presiune atmosferică aproximativ sau 100 kPa), modulul volumetric este de 2100 MPa. Adică, de aproximativ 21.000 de ori mai mare decât presiunea atmosferică.
Din acest motiv, în majoritatea aplicațiilor, lichidele sunt de obicei considerate incompresibile. Acest lucru poate fi verificat imediat cu o aplicație numerică.
-Exercițiu rezolvat 3
Aflați scăderea fracțională a volumului de apă atunci când este supusă unei presiuni de 15 MPa.
Soluţie

Compresibilitatea în gaze
Gazele, așa cum s-a explicat mai sus, funcționează puțin diferit.
Să știe ce volum au n alunitele unui anumit gaz atunci când sunt ținute închise la o presiune P și la o temperatură T, se folosește ecuația de stare. În ecuația de stare pentru un gaz ideal, unde forțele intermoleculare nu sunt luate în considerare, cel mai simplu model afirmă că:
P.Videal = n. R. T
Unde R este constanta ideală a gazului.
Modificările volumului gazului pot fi efectuate la presiune constantă sau temperatură constantă. De exemplu, prin menținerea temperaturii constante, compresibilitatea izotermă ΚT este:

În loc de simbolul „delta” care a fost folosit înainte la definirea conceptului de solide, pentru un gaz este descris cu o derivată, în acest caz derivată parțială cu privire la P, păstrând T constant.
Prin urmare BT modulul de compresibilitate izotermă este:

Și modulul de compresibilitate adiabatic B este, de asemenea, important.adiabatic, pentru care nu există flux de căldură intrat sau ieșit.
Badiabatic = γp
Unde γ este coeficientul adiabatic. Cu acest coeficient, viteza sunetului în aer poate fi calculată:

Aplicând ecuația de mai sus, găsiți viteza sunetului în aer.
Date
Modulul de compresibilitate adiabatică a aerului este de 1,42 × 105 Pa
Densitatea aerului este de 1.225 kg / m3 (la presiune atmosferică și 15 ° C)
Soluţie

În loc să lucreze cu modulul de compresibilitate, ca o schimbare de unitate a volumului per schimbare de presiune, factorul de compresibilitate al unui gaz real, un concept diferit, dar ilustrativ, despre modul în care gazul real se compară cu gazul ideal:
P. Vreal = Z. R. T
Unde Z este coeficientul de compresibilitate al gazului, care depinde de condițiile în care se găsește, fiind în general o funcție atât a presiunii P, cât și a temperaturii T și poate fi exprimat ca:
Z = f (P, T)
În cazul unui gaz ideal Z = 1. Pentru gazele reale valoarea Z crește aproape întotdeauna cu presiunea și scade cu temperatura.
Pe măsură ce presiunea crește, moleculele gazoase se ciocnesc mai frecvent și forțele de respingere dintre ele cresc. Acest lucru poate duce la o creștere a volumului gazului real, prin care Z> 1.
În schimb, la presiuni mai mici, moleculele sunt libere să se miște și predomină forțele de atracție. Într-un astfel de caz, Z < 1.
Pentru cazul simplu al unui mol de gaz n = 1, dacă se mențin aceleași condiții de presiune și temperatură, prin împărțirea ecuațiilor anterioare termen la termen, obținem:

Vreal = Z Videal
-Exercițiu rezolvat 5
Există un gaz real la 250 ° K și 15 atm de presiune, care are un volum molar cu 12% mai mic decât cel calculat prin ecuația de stare a gazului ideal. Dacă presiunea și temperatura sunt menținute constante, găsiți:
a) Factorul de compresibilitate.
b) Volumul molar al gazului real.
c) Ce tip de forțe predomină: atrăgătoare sau respingătoare?
Soluţie
a) Dacă volumul real este cu 12% mai mic decât idealul, înseamnă că:
Vreal = 0,88 Videal
Prin urmare, pentru 1 mol de gaz, factorul de compresibilitate este:
Z = 0,88
b) Alegerea constantei de gaz ideale cu unitățile adecvate pentru datele furnizate:
R = 0,082 L.atm / mol.K
Volumul molar este calculat prin rezolvarea și substituirea valorilor:
c) Predomină forțele atractive, deoarece Z este mai mic de 1.
Referințe
- Atkins, P. 2008. Chimie fizică. Editorial Médica Panamericana. 10 - 15.
- Giancoli, D. 2006. Fizică: principii cu aplicații. 6a. Sala Ed Prentice. 242 - 243 și 314-15
- Mott, R. 2006. Mecanica fluidelor. Pearson Education 13-14.
- Rex, A. 2011. Fundamentele fizicii. Pearson Education. 242-243.
- Tipler, P. (2006) Fizică pentru știință și tehnologie. Ediția a 5-a Volumul 1. Editorial Reverté. 542.


Nimeni nu a comentat acest articol încă.