
Formulele, ecuațiile, exemplele constantelor lui Antoine
Constantele lui Antoine sunt trei parametri care apar într-o relație empirică între presiunea vaporilor de saturație și temperatura substanțelor pure. Acestea depind de fiecare substanță și se presupune că sunt constante într-un anumit interval de temperaturi.
În afara acestui interval, constantele lui Antoine își schimbă valoarea. Constantele sunt legate de o ecuație creată în 1888 de inginerul francez Louis Charles Antoine (1825-1897).
Indice articol
- 1 Formule și ecuații
- 2 aburi de saturație
- 3 Cum se calculează constantele lui Antoine??
- 4 Exemple
- 4.1 Exemplul 1
- 4.2 Exemplul 2
- 4.3 Soluție
- 5 Referințe
Formule și ecuații
Cel mai comun mod de a exprima funcția Antoine este:
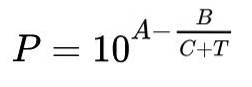
În această formulă P reprezintă presiunea vaporilor de saturație exprimată în milimetri de mercur (mmHg), T este temperatura care a fost variabila independentă și este exprimată în ℃.
A, B și C sunt constantele sau parametrii formulei lui Antoine.
Importanța acestei formule, care, deși este empirică, oferă o expresie analitică simplă, care poate fi ușor utilizată în calculele termodinamice..
Formula lui Antoine nu este unică, există expresii mai precise care sunt extensii ale acestei formule, dar cu dezavantajul că au șase sau mai mulți parametri și că expresia lor matematică este mai complexă, ceea ce le face impracticabile pentru a fi utilizate în calculele termodinamice..
Abur de saturație
Deoarece formula lui Antoine măsoară presiunea de vapori de saturație, este necesar să explicăm în ce constă.
Un lichid este plasat într-o fiolă de sticlă sau alt recipient. Tot aerul este îndepărtat din blister. Ansamblul este plasat într-o baie termică până la atingerea echilibrului..
La început totul este lichid, dar pentru că există vid, moleculele mai rapide încep să părăsească lichidul formând un gaz din aceeași substanță ca lichidul..
Procesul de mai sus este evaporare și pe măsură ce se întâmplă, presiunea vaporilor crește.
Unele dintre moleculele de vapori pierd energie și se reunesc în faza lichidă a substanței, acesta este procesul condensare.
Apoi se produc simultan două procese, evaporarea și condensarea. Când un număr egal de molecule iese din lichidul în care sunt încorporate în el, a echilibru dinamic și în acest moment apare presiunea maximă a vaporilor cunoscută sub numele de presiune de saturație.
Această presiune de saturație a vaporilor o prezice formula lui Antoine pentru fiecare substanță și fiecare temperatură..
În unele solide se produce un fenomen similar atunci când trecem de la faza solidă la faza gazoasă direct fără a trece prin faza lichidă, în aceste cazuri poate fi măsurată și o presiune de vapori de saturație.
Nu este ușor să se stabilească un model teoretic pornind de la primele principii, deoarece sunt implicate schimbări ale energiei cinetice moleculare, care pot fi translaționale, rotaționale și vibraționale, cu energia internă a legăturii moleculare. Din acest motiv se folosesc în practică formule empirice.
Cum se calculează constantele lui Antoine??
Nu există nicio metodă teoretică pentru a obține constantele lui Antoine, deoarece este o relație empirică.
Acestea sunt obținute din datele experimentale ale fiecărei substanțe și ajustând cei trei parametri A, B și C, astfel încât să minimizeze diferența pătratică (metoda celor mai mici pătrate) a predicției cu datele experimentale..
Pentru utilizatorul final, care sunt în general ingineri chimici, există tabele în manualele de chimie în care sunt date aceste constante pentru fiecare substanță, indicând intervalele de temperatură maximă și minimă în care acestea sunt aplicabile..
Există, de asemenea, servicii online care oferă valorile constantelor A, B și C, așa cum este cazul serviciilor online DDBST GmbH.
Poate exista mai multe domenii de temperatură valabile pentru aceeași substanță. Apoi, în funcție de domeniul de lucru, se alege unul sau alt grup de constante.
Pot apărea dificultăți dacă intervalul de lucru al temperaturilor este între două intervale de valabilitate ale constantelor, deoarece predicțiile de presiune ale formulei nu coincid în zona limită.
Exemple
Exemplul 1
Găsiți presiunea de vapori a apei la 25 ℃.
Soluţie
Consultăm tabelele pentru a determina constantele lui Antoine.
Există două game pentru apă:
Între 1 ℃ și 100 ℃ și între 99 ℃ până la 374 ℃.
Deoarece suntem interesați de 25 ℃, luăm prima gamă în care valoarea constantelor lui Antoine este:
A = 8.07131
B = 1730,63
C = 233,426
P = 10 ^ (8.07131 - 1730.63 / (25 + 233.426))
Calculul exponentului
Să calculăm mai întâi exponentul: 1.374499
P = 10 ^ 1,374499 = 23,686 mmHg = 0,031166 atm
Analiza rezultatelor
Aceste rezultate sunt interpretate astfel:
Să presupunem că apa pură este plasată într-un recipient etanș din care aerul a fost îndepărtat cu ajutorul unei pompe de vid..
Recipientul cu apă este plasat într-o baie termică la o temperatură de 25 ℃ până când atinge echilibrul termic..
Apa din recipientul ermetic se evaporă parțial până când atinge presiunea de vapori de saturație, care nu este altceva decât presiunea la care se stabilește echilibrul dinamic dintre faza lichidă a apei și faza de vapori..
Această presiune în acest caz s-a dovedit a fi 0,031166 atm la 25 ℃.
Exemplul 2
Găsiți presiunea de vapori a apei la 100 ℃.
Soluţie
Consultăm tabelele pentru a determina constantele lui Antoine. Există două game pentru apă:
Între 1 ℃ și 100 ℃ și între 99 ℃ până la 374 ℃.
În acest caz, temperatura de interes este în cele două intervale.
Folosim primul interval [1 ℃, 100 ℃]
A = 8.07131
B = 1730,63
C = 233,426
P = 10 ^ (8.07131 - 1730.63 / (100 + 233.426))
Calculul exponentului
Să calculăm mai întâi exponentul: 2.8808
P = 10 ^ 1,374499 = 760,09 mmHg = 1.0001 atm
Apoi folosim al doilea interval [99 ℃, 374 ℃]
În acest caz, constantele sunt
A = 8.14019
B = 1810,94
C = 244,485
P = 10 ^ (8.14019 - 1810.94 / (100 + 244.485))
Să calculăm mai întâi exponentul: 2.88324
P = 10 ^ 2.88324 = 764.2602 mmHg = 1.0056 atm
Există o diferență procentuală între cele două rezultate de 0,55%.
Referințe
- Aplicarea legilor lui Raoult și Dalton și a ecuației lui Antoine. Recuperat de la: misapuntesyantación.wordpress.com
- Calculatorul online al formulei lui Antoine. Recuperat de la: ddbonline.ddbst.de/AntoineCalculation/AntoineCalculationCGI.exe
- Gecousb. Termodinamică și tabele cu abur / constantele lui Antoine. Recuperat de pe: gecousb.com.ve
- Proprietățile termice ale materiei. Recuperat de pe: webserver.dmt.upm.es
- Yaws și Yang. Tabele constante Antoine pentru peste 700 de compuși organici. Recuperat de la: user.eng.umd.edu
- Wikipedia. Ecuația lui Antoine. Recuperat de pe wikipedia.com
- Wikipedia. Ecuația Clausius-Clapeyron. Recuperat de pe wikipedia.com
- Wisniak J. Dezvoltarea istorică a ecuației presiunii vaporilor de la dalton la antoină. Recuperat de pe: link.springer.com


Nimeni nu a comentat acest articol încă.