
Ce este un proces izoterm? (Exemple, exerciții)
proces izotermic sau izotermă este un proces termodinamic reversibil în care temperatura rămâne constantă. Într-un gaz, există situații în care o modificare a sistemului nu produce variații ale temperaturii, ci ale caracteristicilor fizice..
Aceste modificări sunt schimbările de fază, când substanța se schimbă de la solid la lichid, de la lichid la gaz sau invers. În astfel de cazuri, moleculele substanței își reajustează poziția, adăugând sau extragând energie termică..

Energia termică necesară pentru a avea loc o schimbare de fază într-o substanță se numește căldură latentă sau căldură de transformare.
O modalitate de a face izoterm un proces este de a pune substanța care va fi sistemul studiat în contact cu un rezervor termic extern, care este un alt sistem cu o capacitate calorică ridicată. În acest fel, are loc un schimb de căldură atât de lent, încât temperatura rămâne constantă..
Acest tip de proces apare frecvent în natură. De exemplu, la ființele umane, când temperatura corpului crește sau scade, ne simțim rău, deoarece în corpul nostru multe reacții chimice care mențin viața au loc la o temperatură constantă. Acest lucru este valabil pentru animalele cu sânge cald în general..
Alte exemple sunt gheața care se topește la căldură la sosirea primăverii și cuburile de gheață care răcoresc băutura..
Indice articol
- 1 Exemple de procese izoterme
- 1.1 Ciclul Carnot
- 2 Calculul muncii efectuate într-un proces izoterm
- 2.1 - Exercițiul 1
- 2.2 - Exercițiul 2
- 3 Referințe
Exemple de procese izoterme
-Metabolizarea animalelor cu sânge cald are loc la o temperatură constantă.

-Când apa fierbe, are loc o schimbare de fază, de la lichid la gaz, iar temperatura rămâne constantă la aproximativ 100 ° C, deoarece alți factori pot influența valoarea.
-Topirea gheții este un alt proces izoterm comun, la fel ca și plasarea apei în congelator pentru a face cuburi de gheață..
-Motoarele auto, frigiderele, precum și multe alte tipuri de mașini, funcționează corect într-un anumit interval de temperatură. Dispozitive numite termostate. Diferite principii de funcționare sunt utilizate în proiectarea sa.
Ciclul Carnot
Un motor Carnot este o mașină ideală de la care se obține lucrări datorită proceselor complet reversibile. Este o mașină ideală, deoarece nu ia în considerare procesele care disipă energia, cum ar fi vâscozitatea substanței care lucrează, nici fricțiunea.
Ciclul Carnot este format din patru etape, dintre care două sunt exact izoterme, iar celelalte două sunt adiabatice. Etapele izoterme sunt compresia și expansiunea unui gaz care este responsabil pentru producerea de lucrări utile.
Un motor auto funcționează pe principii similare. Mișcarea unui piston în interiorul cilindrului este transmisă către alte părți ale mașinii și produce mișcare. Nu are comportamentul unui sistem ideal precum motorul Carnot, dar principiile termodinamice sunt comune.
Calculul muncii efectuate într-un proces izoterm
Pentru a calcula munca efectuată de un sistem atunci când temperatura este constantă, trebuie să utilizați prima lege a termodinamicii, care spune:
ΔU = Q - W
Acesta este un alt mod de exprimare a conservării energiei în sistem, prezentat prin ΔU sau schimbarea energiei, Î ca căldura furnizată și în cele din urmă W, care este munca depusă de sistemul menționat.
Să presupunem că sistemul în cauză este un gaz ideal conținut în cilindrul unui piston mobil de zonă LA, care funcționează când volumul său V schimbare de V1 la VDouă.

Ecuația de stare a gazului ideal este PV = nRT, care leagă volumul de presiune P și temperatura T. Valorile lui n și R sunt constante: n este numărul de moli ai gazului și R constanta gazelor. În cazul unui proces izoterm, produsul PV este constant.
Ei bine, munca realizată este calculată prin integrarea unei mici lucrări diferențiale, în care o forță F produce un mic offset dx:
dW = Fdx = PAdx
Ce Adx este exact variația volumului dV, atunci:
dW = PdV
Pentru a obține lucrul total într-un proces izotermic, integrăm expresia pentru dW:
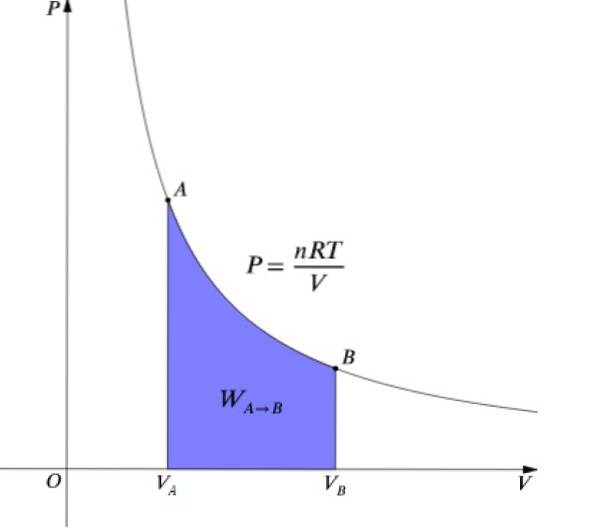
Presiunea P iar volumul V sunt reprezentate grafic într-o diagramă P-V așa cum se arată în figură și munca realizată este egală cu aria de sub curbă:

Ce ΔU = 0 deoarece temperatura rămâne constantă, într-un proces izotermic trebuie:
Q = W
- Exercitiul 1
Un cilindru echipat cu un piston mobil conține un gaz ideal la 127 ° C. Dacă pistonul se mișcă pentru a reduce volumul inițial de 10 ori, menținând temperatura constantă, găsiți numărul de moli de gaz conținut în butelie, dacă lucrarea efectuată pe gaz este de 38.180 J.
Fapt: R = 8,3 J / mol. K
Soluţie
Declarația afirmă că temperatura rămâne constantă, prin urmare suntem în prezența unui proces izoterm. Pentru munca efectuată pe gaz avem ecuația dedusă anterior:

127 º C = 127 + 273 K = 400 K
Rezolvați pentru n, numărul de moli:
n = W / RT ln (V2 / V1) = -38 180 J / 8,3 J / mol. K x 400 K x ln (VDouă/ 10VDouă) = 5 moli
Munca a fost precedată de un semn negativ. Cititorul atent va observa în secțiunea precedentă că W a fost definit ca „lucrare realizată de sistem” și are semnul +. Deci „munca efectuată pe sistem” are un semn negativ.
- Exercițiul 2
Aveți aer într-un cilindru prevăzut cu un piston. Inițial sunt 0,4 m3 de gaz sub presiune 100 kPa și 80 ° C de temperatură. Aerul este comprimat la 0,1 m3 asigurându-se că temperatura din interiorul cilindrului rămâne constantă în timpul procesului.
Stabiliți cât de mult se lucrează în timpul acestui proces.
Soluţie
Folosim ecuația pentru lucru derivat anterior, dar nu se cunoaște numărul de moli, care poate fi calculat cu ecuația gazului ideal:
80 ° C = 80 + 273 K = 353 K.
P1V1 = n.R.T → n = P1V1 / RT = 100000 Pa x 0,4 m3 /8,3 J / mol. K x 353 K = 13,65 mol
W = n.R.T ln (VDouă/ V1) = 13,65 mol x 8,3 J / mol. K x 353 K x ln (0,1 /0,4) = -55,442,26 J
Din nou semnul negativ indică faptul că s-a lucrat la sistem, ceea ce se întâmplă întotdeauna când gazul este comprimat.
Referințe
- Bauer, W. 2011. Fizică pentru inginerie și științe. Volumul 1. Mc Graw Hill.
- Cengel, Y. 2012. Termodinamică. 7ma Ediție. Dealul Mcgraw.
- Figueroa, D. (2005). Seria: Fizică pentru știință și inginerie. Volumul 4. Fluide și termodinamică. Editat de Douglas Figueroa (USB).
- Knight, R. 2017. Fizica pentru oamenii de știință și inginerie: o abordare strategică.
- Serway, R., Vulle, C. 2011. Fundamentele fizicii. 9n / A Cengage Learning.
- Wikipedia. Proces izotermic. Recuperat de pe: en.wikipedia.org.



Nimeni nu a comentat acest articol încă.