
Proprietățile dibenzalacetonei, mecanismul de reacție, utilizări, riscuri
dibenzalacetonă (dba) este un compus organic a cărui formulă moleculară este C17H14O. Este un solid gălbui care, în funcție de puritatea sa, poate apărea sub formă de cristale. Se folosește în produse de protecție solară și în sinteze organometalice în care paladiul este utilizat ca catalizator.
Deși sinteza sa este un proces relativ simplu, destul de recurent în laboratoarele de predare pentru a explica condensarea aldolului, mecanismul său este oarecum extins și trebuie luați în considerare mai mulți factori. Benzaldehida utilizată, care se va condensa cu acetonă, trebuie să fie proaspăt distilată pentru a garanta oxidarea sa scăzută în contact cu aerul..

La fel, un mediu bazic etanol-apă este utilizat pentru a solubiliza reactivii și, în același timp, pentru a promova precipitarea finală a dibenzalacetonei, un compus hidrofob și insolubil. Până în prezent, nu se știe ce efecte negative poate avea dibenzalacetona asupra corpului sau asupra mediului, în afară de faptul că este o substanță iritantă.
Indice articol
- 1 Proprietăți
- 1.1 Aspect fizic
- 1.2 Masa molară
- 1.3 Izomeri
- 1.4 Punct de topire
- 1.5 Solubilitatea în apă
- 1.6 Structura
- 2 Mecanismul de reacție al dibenzalacetonei
- 3 Sinteza
- 3.1 Reactivi
- 3.2 Procedură
- 3.3 Recristalizare
- 4 utilizări
- 5 Riscuri
- 6 Referințe
Proprietăți
Aspectul fizic
Solid gălbui cu aspect de praf sau cristal.
Masă molară
234,29 g / mol
Izomeri
Dibenzalacetona apare ca trei izomeri geometrici: trans-trans, trans-cis și cis-cis. Izomerul trans-trans este cel mai stabil dintre toate și, prin urmare, cel care este cel mai produs în timpul sintezei.
Punct de topire
110-111 ° C. Această gamă variază în funcție de gradul de puritate al solidului sintetizat..
Solubilitatea apei
Insolubil.
Structura
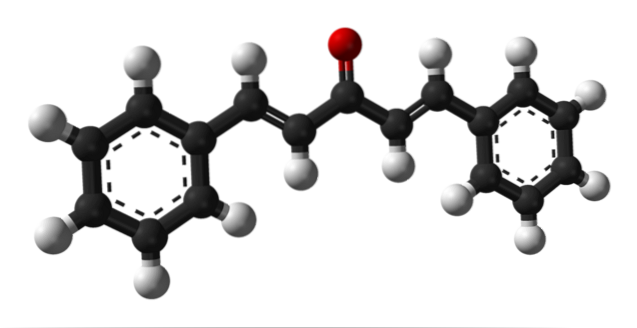
Imaginea superioară arată molecula izomerului trans-trans dibenzalacetonă, reprezentată de un model de sfere și bare. În centrul acesteia avem gruparea carbonil și, pe laturile sale, câteva legături duble și două inele aromatice de benzen.
Dibenzalacetona este în esență apolară și hidrofobă, întrucât întreaga sa structură este compusă practic din atomi de carbon și hidrogen. Gruparea carbonil îi oferă doar un mic moment dipol.
Structura poate fi comparată cu cea a unei frunze, deoarece toți atomii săi de carbon au hibridizare spDouă; prin urmare, se sprijină pe același plan.
Fotonii de lumină interacționează cu sistemul conjugat de dibenzalacetonă; în special cele ale radiațiilor UV, fiind absorbite pentru a excita electronii delocalizați. Această proprietate face dibenzalacetona un excelent absorbant de lumină ultravioletă..
Mecanismul de reacție al dibenzalacetonei
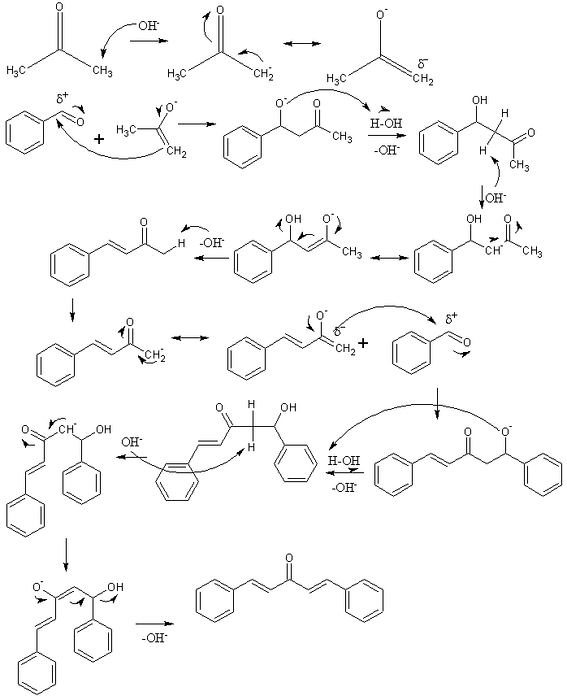
În imaginea superioară am reprezentat mecanismul condensării aldolului între benzaldehidă și acetonă, pentru a provoca astfel dibenzalacetonă; în mod specific, izomerul său trans-trans.
Reacția începe cu acetonă într-un mediu bazic. OH- deprotonează un proton acid al uneia dintre cele două grupări metil, -CH3, dând naștere unui enolat: CH3C (O) CHDouă-, care își delocalizează sarcina negativă prin rezonanță (primul rând al imaginii).
Acest enolat acționează apoi ca un agent nucleofil: atacă gruparea carbonil a unei molecule de benzaldehidă. Incorporarea sa în benzaldehidă generează un alcoxid, care, deoarece este foarte bazic, deprotonează o moleculă de apă și devine aldol (al doilea rând). Aldolul sau β-hidroxicetona se caracterizează prin faptul că are grupele C = O și OH.
Mediul de bază deshidratează acest aldol și se formează o legătură dublă în structura sa, care generează benzilidenacetonă (al treilea rând). Apoi, OH- De asemenea, deprotonează unul dintre hidrogenii săi acizi, repetând un alt atac nucleofil asupra unei a doua molecule de benzaldehidă. De data aceasta atacul are loc cu o viteză mai mică (al patrulea rând).
Produsul format deprotonează o altă moleculă de apă și suferă din nou deshidratare pentru a elimina gruparea OH și a stabili o a doua legătură dublă (rândurile cinci și șase). Astfel și în cele din urmă, se produce dibenzalacetonă.
Sinteză
Reactivi
Reactivii pentru efectuarea sintezei dibenzalacetonei sunt următorii:
- 95% etanol.
- Benzaldehidă proaspăt distilată din ulei de migdale amare.
- NaOH ca catalizator de bază în apă distilată.
Cantitățile care trebuie utilizate depind de câtă dibenzalacetonă trebuie sintetizată. Cu toate acestea, se caută existența unui exces de benzaldehidă, deoarece o parte din aceasta este oxidată la acid benzoic. De asemenea, este garantat că reacția durează mai puțin timp și că benzilidenacetona nedorită este produsă într-o măsură mai mică..
Etanolul acționează ca solvent pentru benzaldehidă, altfel nu s-ar dizolva în mediul NaOH bazic.
Proces
Într-un pahar mare, amestecați etanolul cu benzaldehida. Apoi, se adaugă mediul de bază NaOH în timpul agitării magnetice constante. În acest pas, reacția Cannizzaro are loc într-un grad mai mic; adică două molecule de benzaldehidă disproporționate într-una din alcool benzilic și cealaltă din acid benzoic, ușor de recunoscut prin mirosul său caracteristic dulce.
În cele din urmă, se adaugă acetonă și soluția este așteptată o jumătate de oră pentru a deveni tulbure și de culoare galben-portocalie. Dibenzalacetona va precipita din cauza apei, astfel încât se adaugă un volum considerabil de apă pentru a promova precipitația sa completă..
Dibenzalacetona este filtrată sub vid și solidul său gălbui se spală de mai multe ori cu apă distilată..
Recristalizare

Pentru purificarea dibenzalacetonei, se utilizează etanol 95% sau acetat de etil fierbinte, astfel încât se obțin cristale de puritate mai mare de fiecare dată când se repetă recristalizarea. Astfel, pulberea gălbuie inițială va fi transformată în mici cristale galbene de dibenzalacetonă..
Aplicații
Dibenzalacetona este un compus care nu are multe utilizări. Datorită capacității sale de a absorbi lumina ultravioletă, este utilizat în formularea de protecție solară sau a oricărui alt produs care urmărește atenuarea incidenței razelor UV, fie că este vorba de acoperiri sau vopsele..
Pe de altă parte, dibenzalacetona este utilizată în sintezele organometalice de paladiu. Acționează ca un liant care se coordonează cu atomii de paladiu metalici, Pd0, pentru a forma complexul tris (dibenzilideneacetonă) dipaladiu (0).
Acest compus organometalic furnizează atomi de Pd0 în diferite sinteze organice, deci se comportă ca un catalizator omogen, deoarece se dizolvă în mulți solvenți organici.
De asemenea, dibenzalacetona ca liant este ușor de înlocuit cu alți lianți organici, ceea ce permite sintezelor organometalice de paladiu să se dezvolte rapid..
Riscuri
În ceea ce privește riscurile, nu există prea multe informații disponibile care să raporteze posibilele efecte asupra sănătății sau mediului pe care dibenzalacetona le poate provoca. În stare pură, este un iritant solid prin ingestie, respirație sau prin contact direct cu ochii sau pielea..
Cu toate acestea, se pare că nu este suficient de iritant încât să nu poată face parte din formulările de protecție solară. Pe de altă parte, fiind atât de insolubil în apă, concentrația sa în aceasta este neglijabilă, prezentându-se ca un contaminant solid. În acest sens, nu se știe cât de dăunătoare este turbiditatea pe care o provoacă faunei sau solurilor marine..
Până când nu se dovedește contrariul, dibenzalacetona va fi considerată un compus relativ sigur, deoarece reactivitatea sa scăzută nu este un motiv de risc sau precauții mai mari..
Referințe
- Morrison, R. T. și Boyd, R, N. (1987). Chimie organica. Ediția a V-a. Editorial Addison-Wesley Interamericana.
- Carey F. (2008). Chimie organica. (Ediția a șasea). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimie organica. (Ediția a X-a.). Wiley plus.
- Wikipedia. (2020). Dibenzilideneacetonă. Recuperat de pe: en.wikipedia.org
- Centrul Național pentru Informații despre Biotehnologie. (2020). Dibenzilideneacetonă. Baza de date PubChem., CID = 640180. Recuperat de la: pubchem.ncbi.nlm.nih.gov
- Sinteze organice. (2020). Dibenzalacetonă. Recuperat de pe: orgsyn.org
- Dibenzalacetonă prin condensare Aldol. Recuperat de pe: web.mnstate.edu


Nimeni nu a comentat acest articol încă.