
Caracteristicile, funcțiile, componentele porilor nucleari
porul nuclear (din greacă, porii = trecere sau tranzit) este „poarta” nucleului care permite cea mai mare parte a transportului între nucleoplasmă și citoplasmă. Porul nuclear se alătură membranelor interioare și exterioare ale nucleului pentru a forma canale, care servesc la transportul proteinelor și ARN-ului.
Cuvântul por nu reflectă complexitatea structurii în cauză. Din această cauză, este de preferat să ne referim la complexul porilor nucleari (CPN), mai degrabă decât la porii nucleari. CPN poate suferi modificări în structura sa în timpul transportului sau stări ale ciclului celular.
Recent, s-a descoperit că nucleoporinele, proteinele care alcătuiesc CPN, au un rol important în reglarea expresiei genelor. Astfel, atunci când apar mutații care afectează funcția nucleoporinelor, la om apar patologii, cum ar fi bolile autoimune, cardiomiopatiile, infecțiile virale și cancerul..
Indice articol
- 1 Caracteristici
- 2 Funcții
- 2.1 Importul de substanțe
- 2.2 Exportul de substanțe
- 2.3 Transport ARN
- 2.4 Complexul porilor nucleari și controlul expresiei genelor
- 2.5 Complexul porilor nucleari și virologia
- 3 componente
- 4 Referințe
Caracteristici
Prin tomografie electronică s-a determinat că CPN are o grosime de 50 nm, un diametru extern între 80 și 120 nm și un diametru intern de 40 nm. Moleculele mari, cum ar fi subunitatea mare a ribozomului (MW 1590 kDa), pot fi exportate din nucleu prin CPN. Se estimează că există între 2.000 și 4.000 de NPC-uri pe nucleu.
Greutatea moleculară a unei CPN individuale este aproximativ între 120 și 125 MDa (1 MDa = 106 Da) la vertebrate. În schimb, CPN este mai mic în drojdie, în care este de aproximativ 60 MDa. În ciuda dimensiunii enorme a CPN, nucleoporinele sunt foarte conservate în toate eucariotele.
Translocarea prin CPN este un proces rapid, a cărui viteză este de 1000 de translocații / secundă. Cu toate acestea, CPN în sine nu determină direcția fluxului de transport..
Depinde de gradientul RanGTP, care este mai mare în nucleu decât în citosol. Acest gradient este menținut de un factor de schimb de guanină Ran.
În timpul ciclului celular, CPN-urile suferă cicluri de asamblare și dezunificare a componentelor lor. Asamblarea are loc la interfață și imediat după mitoză.
Caracteristici
Acidul ribonucleic (ARN nuclear mic, ARN mesager, ARN de transfer), proteine și ribonucleoproteine (RNP) trebuie transportat activ prin CPN. Aceasta înseamnă că este necesară energia din hidroliza ATP și GTP. Fiecare moleculă este transportată într-un mod specific.
În general, moleculele de ARN sunt ambalate cu proteine care formează complexe RNP, fiind exportate în acest fel. În schimb, proteinele care sunt transportate activ către nucleu trebuie să posede o secvență semnal de localizare a nucleului (SLN), posedând reziduuri de aminoacizi încărcate pozitiv (de exemplu, KKKRK)..
Proteinele care sunt exportate în nucleu trebuie să aibă un semnal de export al nucleului (NES) bogat în aminoacid leucina..
Pe lângă facilitarea transportului între nucleu și citoplasmă, CPN sunt implicate în organizarea cromatinei, reglarea expresiei genelor și repararea ADN-ului. Nucleoporinele (Nups) promovează activarea sau reprimarea transcripției, indiferent de starea de proliferare celulară.
În drojdie, Nups se găsesc în CNP a anvelopei nucleare. În metazoane se găsesc în interior. Ei îndeplinesc aceleași funcții în toate eucariotele.
Importul de substanțe
Prin CPN există difuzie pasivă a moleculelor mici în ambele direcții și transport activ, import de proteine, export de ARN și ribonucleoproteine (RNP) și naveta bidirecțională de molecule. Acesta din urmă include ARN, RNP și proteine implicate în semnalizare, biogeneză și rotație..
Importul proteinelor în nucleu are loc în două etape: 1) legarea proteinei de partea citoplasmatică a CPN; 2) translocare dependentă de ATP prin CPN. Acest proces necesită hidroliza ATP și schimbul de GTP / PIB între nucleu și citoplasmă..
Conform unui model de transport, complexul receptor-proteină se deplasează de-a lungul canalului prin legare, disociere și reatașare la secvențele FG repetate ale nucleoporinelor. În acest fel, complexul se mută de la o nucleoporină la alta în cadrul CPN..
Exportul de substanțe
Este similar cu importul. Ran GTPase impune direcționalitatea transportului prin CNP. Ran este un comutator molecular cu două stări conformaționale, în funcție de faptul că este legat de PIB sau GTP.
Două proteine de reglare specifice Ran determină conversia între cele două stări: 1) proteina activatoare citosolică a GTPazei (GAP), care determină hidroliza GTP și astfel convertește Ran-GTP în Ran-GDP; și 2) factorul de schimb de guanină nucleară (GEF), care promovează schimbul de PIB pentru GTP și convertește Ran-PIB în Ran-GTP.
Citosolul conține în principal Ran-GDP. Nucleul conține în principal Ran-GTP. Acest gradient al celor două forme conformaționale ale Ran direcționează transportul în direcția corespunzătoare..
Importarea receptorului, atașat la marfă, este facilitată de atașarea la repetițiile FG. Dacă ajunge la partea nucleară a CNP, Ran-GTP se alătură receptorului în eliberarea poziției sale. Astfel, Ran-GTP creează direcția procesului de import.
Exportul nuclear este similar. Cu toate acestea, Ran-GTP din nucleu promovează legarea încărcăturii de receptorul de export. Când receptorul de export se deplasează prin por în citosol, acesta întâlnește Ran-GAP, care induce hidroliza GTP la PIB. În cele din urmă, receptorul este eliberat din post și Ran-GDP în citosol..
Transport ARN
Exportul unor clase de ARN este similar cu exportul de proteine. De exemplu, tARN și nsARN (nucleare mici) utilizează gradientul RanGTP și sunt transportate prin CPN de către carioferină exportin-t și respectiv Crm. Exportul de ribozomi maturi este, de asemenea, dependent de gradientul RanGTP.
MRNA este exportat într-un mod foarte diferit de proteine și alte ARN-uri. Pentru exportul său, ARNm formează un complex de RNP messenger (mRNP), în care o moleculă de ARNm este înconjurată de sute de molecule de proteine. Aceste proteine au funcția de prelucrare, plafonare, splicarea și poliadenilarea ARNm.
Celula trebuie să poată distinge între ARNm cu ARNm matur și ARNm cu ARNm imatur. ARNm, care formează complexul RPNm, ar putea adopta topologii care trebuie remodelate pentru transport. Înainte ca mRNP să intre în CPN, are loc o etapă de control efectuată de complexele proteice TRAMP și exosom..
Când RNPm matur este asamblat, RPNm este transportat prin canal de un receptor de transport (Nxf1-Nxt1). Acest receptor are nevoie de hidroliza ATP (nu un gradient RanGTP) pentru a stabili direcționalitatea de remodelare a mRNP, care va ajunge la citoplasmă.
Complexul porilor nucleari și controlul expresiei genelor
Unele studii indică faptul că componentele CPN ar putea influența reglarea expresiei genelor controlând structura cromatinei și accesibilitatea acesteia la factorii de transcripție..
În eucariotele evoluate mai recent, heterocromatina este localizată preferențial la periferia nucleului. Acest teritoriu este întrerupt de canalele de eucromatină, care sunt întreținute de coșul nuclear al CPN. Asocierea coșului nuclear cu euchromatina este legată de transcrierea genelor.
De exemplu, activarea transcripției la nivelul CPN implică interacțiunea componentelor coșului nuclear cu proteine precum histona SAGA acetiltransferază și factorii de export de ARN..
Astfel, coșul nuclear este o platformă pentru numeroase gene de menaj (menaj) foarte transcrise și gene puternic induse de modificările condițiilor de mediu.
Complexul porilor nucleari și virologia
Infecția virală cu celule eucariote depinde de CPN. În fiecare caz de infecție virală, succesul acesteia depinde de ADN, ARN sau RPN care trece prin CPN pentru a-și atinge scopul final, care este replicarea virusului..
Virusul simian 40 (SV40) a fost unul dintre cele mai studiate modele de investigare a rolului CPN în translocația în nucleu. Acest lucru se datorează faptului că SV40 are un genom mic (5.000 de baze).
S-a demonstrat că transportul ADN-ului virusului este facilitat de proteinele de acoperire a virusului, care protejează virusul până ajunge la nucleu..
Componente (editați)
CPN este încorporat în anvelopa nucleară și este format din aproximativ 500 și 1000 Nups, aproximativ. Aceste proteine sunt organizate în subcomplexe structurale sau module, care interacționează între ele..
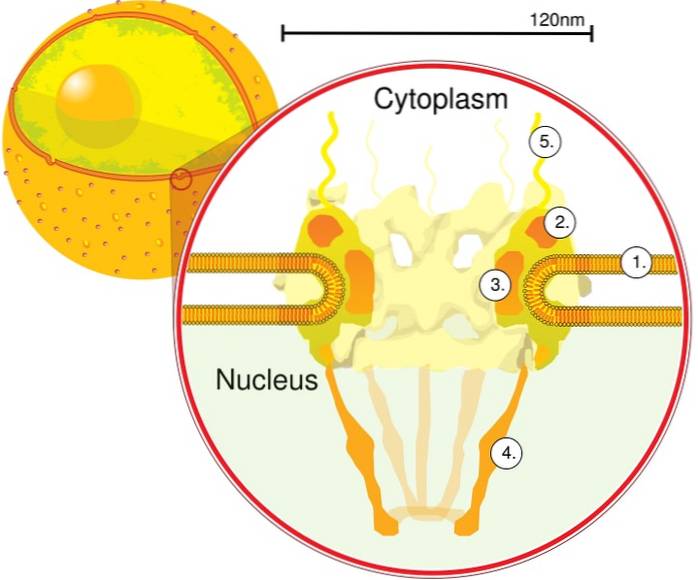
Primul modul este o componentă centrală, sau inel, în interiorul porului în formă de clepsidră, care este delimitat de un alt inel de 120 nm în diametru pe ambele fețe, intranucleare și citoplasmatice. Al doilea modul este nucleul și inelele de citoplasmă (cu diametrul de 120 nm fiecare) situate în jurul componentei în formă de clepsidră..
Al treilea modul este format din opt filamente care se proiectează din inelul de 120 nm în nucleoplasmă și formează o structură în formă de coș. Al patrulea modul este alcătuit din filamente care se proiectează spre partea citoplasmei..
Complexul în formă de Y, alcătuit din șase Nups și proteinele Seh 1 și Sec 13, este cel mai mare și cel mai bine caracterizat complex al CNP. Acest complex este unitatea esențială care face parte din schela CPN.
În ciuda similitudinii reduse dintre secvențele Nups, schela CPN este foarte conservată în toate eucariotele.
Referințe
- Beck, M., Hurt, E. 2016. Complexul porilor nucleari: înțelegerea funcției sale prin o perspectivă structurală. Nature Reviews, Molecular Cell Biology, Doi: 10.1038 / nrm.2016.147.
- Ibarra, A., Hetzer, M.W. 2015. Proteinele porilor nucleari și controlul funcțiilor genomului. Gene și dezvoltare, 29, 337-349.
- Kabachinski, G., Schwartz, T.U. 2015. Complexul porilor nucleari - structură și funcție dintr-o privire. Journal of Cell Science, 128, 423-429.
- Knockenhauer, K.E., Schwartz, T.U. 2016. Complexul porilor nucleari ca o poartă flexibilă și dinamică. Cell, 164, 1162-1171.
- Ptak, C., Aitchison, J.D., Wozniak, R.W. 2014. Complexul multifuncțional al porilor nucleari: o platformă pentru controlul expresiei genelor. Avizul actual al biologiei celulare, DOI: 10.1016 / j.ceb.2014.02.001.
- Stawicki, S.P., Steffen, J. 2017. Republicare: complexul porilor nucleari - o revizuire cuprinzătoare a structurii și funcției. Revista Internațională de Medicină Academică, 3, 51-59.
- Tran, E.J., Wente, S.R. 2006. Complexe dinamice de pori nucleari: viață la margine. Cell, 125, 1041-1053.



Nimeni nu a comentat acest articol încă.