
Caracteristicile sincițiotrofoblastelor, funcția, apoptoza placentară
sinciotrofoblast Este o masă citoplasmatică multinucleată care formează stratul exterior al trofoblastului și intră în contact cu țesutul matern. Acest strat celular se găsește invadând epiteliul și stroma endometrului în timpul dezvoltării embrionare a mamiferelor. Celulele care alcătuiesc sinctiotrofoblastul se fuzionează între ele, pierzându-și membranele celulare.
Acest strat de celule provine din diferențierea celulară a citotrofoblastului și este responsabil pentru schimbul de gaze și substanțe nutritive între mamă și făt. În plus, este capabil să producă hormoni și peptide în faza de implantare a blastocistului către endometru și formarea placentei..
Indice articol
- 1 Caracteristici
- 2 Rol în dezvoltarea embrionară
- 2.1 Nidarea sau implantarea
- 2.2 Circulația utero-placentară
- 3 Apoptoza placentară
- 3.1 Apoptoza și preeclampsia
- 3.2 Dovezi ale relației dintre apoptoză și preeclampsie
- 4 Referințe
Caracteristici
După cum sugerează și numele, celulele sinciotrofoblaste și-au pierdut membranele și s-au contopit, dând acestui strat celular un aspect multicleat asemănător sincițial..
Aceste celule acoperă continuu suprafața viloasă corionică, decidua bazală și placa corionică și fac parte din bariera placentară responsabilă de separarea sângelui mamei și a sângelui fetal..
Sinctiotrofoblastul provine din proliferarea și fuziunea celulelor citotrofoblaste. Celulele acestui strat nu au capacitate proliferativă, adică nu suferă mitoză, deci extinderea și menținerea acestui strat celular depinde doar de încorporarea continuă a celulelor din citotrofoblast, asigurându-i funcționalitatea..
Aceste celule au complexe Golgi și reticul endoplasmatic abundent neted și aspru, precum și un număr mare de incluziuni de mitocondrii și lipide..
Acest strat de celule are, de asemenea, o funcție secretorie, eliberând progesteron, estrogen, gonadotropină corionică umană (hCG) și lactogeni. Pe măsură ce materialul celular îmbătrânește, acesta este înfășurat într-o membrană de protecție și eliminat prin circulația maternă..
Rol în dezvoltarea embrionară
Nidarea sau implantarea
Blastocistul se alătură endometrului declanșând o etapă de proliferare rapidă a celulelor, cu diferențierea trofoblastului în citotrofoblast și sinciotrofoblast. Acesta din urmă se extinde prin epiteliul endometrial până ajunge la stroma sa, unde celulele se umplu cu lipide și glicogen, devenind celule deciduale..
Aceste celule deciduale suferă procese degenerative care le permit să furnizeze substanțe nutritive embrionului în curs de dezvoltare..
Odată ce blastocistul este implantat în endometru prin procesul de implantare sau cuibărire, fuziunea celulelor exterioare ale trofoblastului, dă naștere sincitiotrofoblastului primitiv.
Ulterior, se formează lagune, ocupate de secreții glandulare ale endometrului, care ulterior vor fi înlocuite cu sânge matern, prin slăbirea vaselor capilare și a venulelor endometriale..
Aceste lacune intracelulare umplute cu sânge matern definesc faza lacunară sau trabeculară și se extind până ajung în partea opusă a punctului de implantare..
Lacunele din sinctiotrofoblast se numesc trabecule. Embriogeneza, care constă în modificări ale embrioblastului din interiorul blastocistului, apare și în acest stadiu..
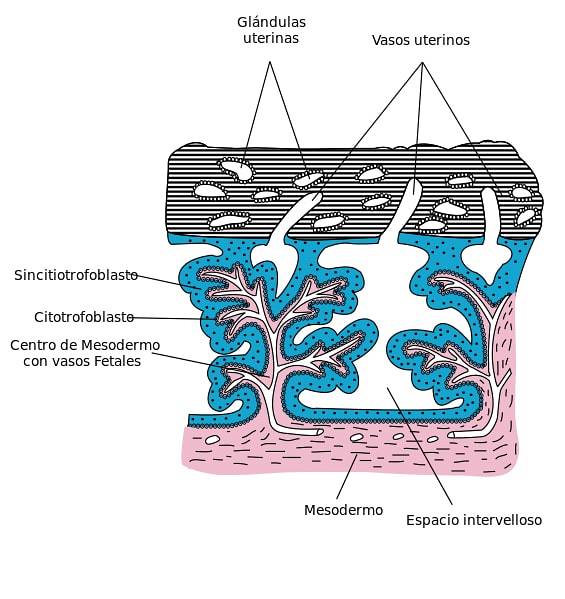
Circulația utero-placentară
Una dintre funcțiile fundamentale ale sinciotrofoblastului este schimbul metabolic între mamă și făt, demonstrând o activitate endocrină ridicată și participând la homeostazia dezvoltării embrionare..
Apariția lacunelor intracelulare sau trofoblastice în sincitiotrofoblast inițiază dezvoltarea circulației utero-placentare. Sinusoidele derivate din capilarele porțiunii materne a placentei curg în aceste lagune..
Un flux direcțional este format de presiunea diferențială dintre vasele circulatorii și lagunele trofoblastice. Acest flux merge de la artere la vene, formând circulația utero-placentară primitivă..
Există un transfer de substanțe nutritive de la vasele materne la embrion, ceea ce este evident la observarea abundentei vezicule pinocitice ale sinciotrofoblastului..
Stratul celular sincițial aliniază vilozitățile plutitoare ale placentei. Aceste vilozități intră în contact cu sângele matern atunci când se stabilește circulația utero-placentară, reglând astfel transportul oxigenului și nutrienților..
Apoptoza placentară
Apoptoza sau moartea celulară programată se dovedește a fi o componentă importantă în dezvoltarea embrionară, astfel are loc eliminarea celulelor selectate, pentru a preveni pierderea nediscriminată a celulelor. Fuziunea sincițială a celulelor citotrofoblaste este faza inițială a cascadei apoptotice.
În stadiul inițial al apoptozei, celulele citotrofoblaste proliferează și fuzionează pentru a forma stratul sincițial sau sinciotrofoblastul..
În faza de execuție a apoptozei, materialul citoplasmatic și nucleic al citotrofoblastului a trecut în stratul sincițial, deci celulele acestui ultim strat sunt echipate cu materialul necesar pentru a începe cascada apoptotică..
Procesul apoptotic prezintă o pauză temporară datorită acțiunii enzimelor antiapoptotice, cu toate acestea, enzima caspază 3 reactivează acest proces, deoarece activează la rândul său componente care degradează proteinele și acizii nucleici din celule. Sunt activate alte enzime responsabile de degradarea microfilamentelor celulare.
După degradarea componentelor celulare, deșeurile sunt ambalate în membranele apicale ale sinciotrofoblastului, originând nodurile sincițiale sau apoptotice, care vor fi în cele din urmă eliberate în fluxul sanguin al mamei..
Apoptoza și preeclampsia
Preeclampsia este o patologie prezentată în timpul sarcinii. Unele cercetări au arătat că această patologie este cauzată de o modificare a diferențierii trofoblastului datorită unui exces de procese apoptotice la acest nivel..
Eliberarea deșeurilor apoptotice în fluxul sanguin matern nu provoacă răspunsuri inflamatorii la mamă deoarece aceste deșeuri sunt protejate de o membrană care le împiedică să intre în contact cu structurile materne. Procesul de acoperire a resturilor durează câteva săptămâni.
În preeclampsie, există un exces de proliferare și fuziune a celulelor citotrofoblaste, ceea ce determină o creștere a degradării celulare a sinciotrofoblastului. Această creștere provoacă o acumulare de resturi celulare și o întârziere în formarea membranei lor de protecție..
Acest lucru face ca resturile și microfragmentele parțial degradate, inclusiv enzimele sincitiotrofoblaste să pătrundă în sângele mamei, provocând leziuni tisulare. Pe lângă preeclampsie, stările hipoxice din placentă au fost asociate cu o creștere a apoptozei celulare.
Dovezi pentru relația dintre apoptoză și preeclampsie
La pacienții cu preeclampsie s-au găsit concentrații citoplasmatice semnificative de microfragmente ale sinciotrofoblastului. Aceste microfragmente pot modifica comportamentul macrofagelor, provocând atât o activare crescută a neutrofilelor, cât și o relaxare endotelială scăzută..
Aceste modificări ale celulelor sanguine materne explică afectarea sistemică și manifestarea preeclampsiei, care provoacă leziuni epiteliale și un răspuns inflamator. În plus față de a provoca leziuni ale placentei din cauza creșterii depunerilor de fibrinoizi pe vilozități.
Referințe
- Flores, A. M., Montoya, J. B., Aguilar, A. O. și Ortega, F. V. (2006). Dezvoltarea și validarea unui model de cultură in vitro pentru studiul diferențierii trofoblastului uman. Ginecologie și obstetrică din Mexic, 74 (12), 657-665.
- Hernández-Valencial, M., Valencia-Ortega, J., Ríos-Castillo, B., Cruz-Cruz, P. D. R. și Vélez-Sánchez, D. (2014). Elemente de implantare și placentare: aspecte clinice și meleculare. Revista mexicană de medicină a reproducerii, 6 (2), 102-116.
- Reece, E. A. și Hobbins, J. C. (2010). Obstetrică clinică / Obstetrică clinică. Panamerican Medical Ed..
- Rodríguez, M., Couve, C., Egaña, G. și Chamy, V. (2011). Apoptoza placentară: mecanisme moleculare în geneza preeclampsiei. Revista chiliană de obstetrică și ginecologie, 76 (6), 431-438.
- Ross, M. H. și Pawlina, W. (2007). Histologie. Panamerican Medical Ed..
- Roura, L. C. (2007). Obstetrică și medicină materno-fetală. Panamerican Medical Ed..



Nimeni nu a comentat acest articol încă.